题目内容
(2013?河东区二模)尿素(H2NCONH2)是一种非常重要的高氮化肥,在工农业生产中有着非常重要的地位.
(1)工业上合成尿素的反应如下:2NH3(l)+CO2(g)?H2O(l)+H2NCONH2(l)△H=-103.7kJ?mol-1
下列措施中有利于提高尿素的生成速率的是
A.采用高温 B.采用高压
C.寻找更高效的催化剂 D.减小体系内CO2浓度
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)?H2NCOONH4(氨基甲酸铵)(l)△H1
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(l)△H2.
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和l mol二氧化碳,实验测得反应中各组分随时间的变化如下图I所示:
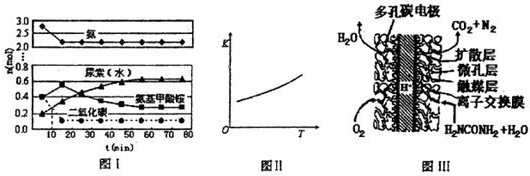
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
②第二步反应的平衡常数K随温度的变化如上图II所示,则△H2
(3)在温度70-95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2
①尿素与NO、NO2三者等物质的量反应,化学方程式为
②已知:N2(g)+O2(g)═2NO(g).△H=180.6kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=
(4)尿素燃料电池结构如上图III所示.其工作时负极电极反应式可表示为
(1)工业上合成尿素的反应如下:2NH3(l)+CO2(g)?H2O(l)+H2NCONH2(l)△H=-103.7kJ?mol-1
下列措施中有利于提高尿素的生成速率的是
ABC
ABC
A.采用高温 B.采用高压
C.寻找更高效的催化剂 D.减小体系内CO2浓度
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)?H2NCOONH4(氨基甲酸铵)(l)△H1
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(l)△H2.
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和l mol二氧化碳,实验测得反应中各组分随时间的变化如下图I所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
2
2
步反应决定,总反应进行到55
55
min时到达平衡.②第二步反应的平衡常数K随温度的变化如上图II所示,则△H2
>
>
0(填“>”“<”或“=”)(3)在温度70-95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2
①尿素与NO、NO2三者等物质的量反应,化学方程式为
CO(NH2)2+NO+NO2=CO2+2N2+2H2O
CO(NH2)2+NO+NO2=CO2+2N2+2H2O
.②已知:N2(g)+O2(g)═2NO(g).△H=180.6kJ?mol-1
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=
-1627.2
-1627.2
kJ?mol-1(4)尿素燃料电池结构如上图III所示.其工作时负极电极反应式可表示为
CO(NH2)2+H2O-6e-=CO2+N2+6H+
CO(NH2)2+H2O-6e-=CO2+N2+6H+
.分析:(1)依据化学反应的反应特征,影响化学反应速率的因素分析判断;
(2)①已知总反应的快慢由慢的一步决定,结合图象变化趋势,图象表达反应的判断,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;当氨基甲酸铵,尿素物质的量不再变化时,反应达到平衡;
②依据化学平衡常数的表达意义和计算分析判断平衡移动方向;
(3)①依据原子守恒配平
②依据热化学方程式和盖斯定律计算得到;
(4)尿素燃料电池依据原电池原理,燃料在负极发生氧化反应,氧气再正极得到电子发生还原反应;结合图中生成产物写出电极反应.
(2)①已知总反应的快慢由慢的一步决定,结合图象变化趋势,图象表达反应的判断,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;当氨基甲酸铵,尿素物质的量不再变化时,反应达到平衡;
②依据化学平衡常数的表达意义和计算分析判断平衡移动方向;
(3)①依据原子守恒配平
②依据热化学方程式和盖斯定律计算得到;
(4)尿素燃料电池依据原电池原理,燃料在负极发生氧化反应,氧气再正极得到电子发生还原反应;结合图中生成产物写出电极反应.
解答:解:(1)2NH3(l)+CO2(g)?H2O(l)+H2NCONH2(l)△H=-103.7kJ?mol-1 ,反应是放热反应,反应前后气体体积减小;有利于提高尿素的生成速率需要依据影响化学反应速率的因素进行分析,
A.采用高温,反应是放热反应,平衡逆向进行,但反应速率增大,故A符合;
B.反应由气体参加,反应前后气体体积减小,采用高压,增大压强,反应正向进行,反应速率增大,故B符合;
C.寻找更高效的催化剂,催化剂可以加快反应速率,但不改变平衡,故C符合;
D.减小体系内CO2浓度平衡逆向进行,反应速率减小,故D不符合;
故答案为:ABC;
(2)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二部反应,从曲线斜率不难看出第二部反应速率慢,所以已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第二步决定,由图象变化可知当进行到55分钟时,反应达到平衡,
故答案为:2;55;
②第二步反应的平衡常数K随温度的升高增大,说明反应是吸热反应,△H2>0,故答案为:>;
(3)①工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2,尿素与NO、NO2三者等物质的量反应,生成二氧化碳、氮气和水,反应的化学方程式为:CO(NH2)2+NO+NO2=CO2+2N2+2H2O,故答案为:CO(NH2)2+NO+NO2=CO2+2N2+2H2O;
②a、N2(g)+O2(g)═2NO(g).△H=180.6kJ?mol-1
b、N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
c、2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
依据盖斯定律c×3-2×b-2×a得到,4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=-1627.2KJ/mol,故答案为:1627.2KJ/mol;
(4)依据尿素燃料电池结构,尿素在负极发生氧化反应失电子生成二氧化碳和氮气,氧气在正极得到电子发生还原反应生成氢氧根离子,酸性介质中实际生成水,负极电极反应为:
CO(NH2)2+H2O-6e-=CO2+N2+6H+;正极电极反应为O2+4H++4e-=2H2O,故答案为:CO(NH2)2+H2O-6e-=CO2+N2+6H+.
A.采用高温,反应是放热反应,平衡逆向进行,但反应速率增大,故A符合;
B.反应由气体参加,反应前后气体体积减小,采用高压,增大压强,反应正向进行,反应速率增大,故B符合;
C.寻找更高效的催化剂,催化剂可以加快反应速率,但不改变平衡,故C符合;
D.减小体系内CO2浓度平衡逆向进行,反应速率减小,故D不符合;
故答案为:ABC;
(2)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二部反应,从曲线斜率不难看出第二部反应速率慢,所以已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第二步决定,由图象变化可知当进行到55分钟时,反应达到平衡,
故答案为:2;55;
②第二步反应的平衡常数K随温度的升高增大,说明反应是吸热反应,△H2>0,故答案为:>;
(3)①工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2,尿素与NO、NO2三者等物质的量反应,生成二氧化碳、氮气和水,反应的化学方程式为:CO(NH2)2+NO+NO2=CO2+2N2+2H2O,故答案为:CO(NH2)2+NO+NO2=CO2+2N2+2H2O;
②a、N2(g)+O2(g)═2NO(g).△H=180.6kJ?mol-1
b、N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1
c、2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
依据盖斯定律c×3-2×b-2×a得到,4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=-1627.2KJ/mol,故答案为:1627.2KJ/mol;
(4)依据尿素燃料电池结构,尿素在负极发生氧化反应失电子生成二氧化碳和氮气,氧气在正极得到电子发生还原反应生成氢氧根离子,酸性介质中实际生成水,负极电极反应为:
CO(NH2)2+H2O-6e-=CO2+N2+6H+;正极电极反应为O2+4H++4e-=2H2O,故答案为:CO(NH2)2+H2O-6e-=CO2+N2+6H+.
点评:本题考查了化学平衡的影响因素分析,化学反应速率的影响因素判断,图象分析反应的进行程度,热化学方程式和盖斯定律的计算应用,原电池电极反应书写的方法,题目难度中等.

练习册系列答案
相关题目
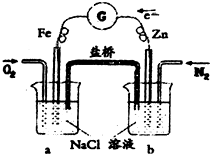 (2013?河东区二模)如图所示,下列判断中正确的是( )
(2013?河东区二模)如图所示,下列判断中正确的是( )