题目内容
【题目】将100 mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。则下列判断中错误的是
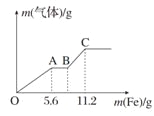
A.OA段产生的气体是NO,BC段产生的气体是H2
B.A点对应消耗NO3-物质的量为0.1 mol
C.B点对应消耗铁粉的质量为8.4 g
D.原混合酸溶液中H2SO4的浓度为2.0 mol·L-1
【答案】D
【解析】
A. 向另一份中逐渐加入铁粉,硝酸首先把铁氧化为硝酸铁、自身被还原为NO,同时还产生水,当硝酸完全被消耗后,继续加入铁粉,铁与溶液中的铁离子反应生成亚铁离子,当铁离子完全消耗后,加入的铁粉与溶液中的氢离子反应生成氢气,因此OA段产生的气体是NO,BC段产生的气体是H2,A正确;
B. A点硝酸根恰好完全被消耗,消耗铁的物质的量是5.6g÷56g/mol=0.1mol,Fe失去0.3mol电子,则根据电子得失守恒可知消耗硝酸的物质的量是0.1mol,因此对应消耗NO3-物质的量为0.1 mol,B正确;
C. 根据B项分析,A点生成0.1molFe3+,根据方程式2Fe3++Fe=3Fe2+可知0.1mol铁离子消耗0.05mol铁,则B点对应消耗铁粉的质量为(0.1mol+0.05mol)×56g/mol=8.4 g,C正确;
D. 最终消耗铁是11.2g,物质的量是11.2g÷56g/mol=0.2mol,则溶液中产生硫酸亚铁是0.2mol,根据S原子守恒可知,每一份溶液中硫酸的物质的量是0.2mol,硫酸的浓度是0.2mol÷0.05L=4mol/L,D错误;
答案选D。

【题目】常温下①、②两个装有50mL氯气的针筒,分别抽取10mLH2O和10mL15%的NaOH溶液(如图所示),充分振荡后静置,对两针筒中所得溶液描述错误的是

A | B | C | D | |
针筒① | 有颜色 | 有漂白性 | 呈酸性 | 含Cl2分子 |
针筒② | 无颜色 | 无漂白性 | 呈碱性 | 无Cl2分子 |
A. AB. BC. CD. D