题目内容
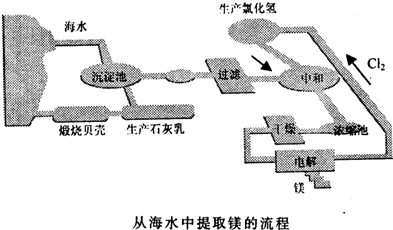
海水中含有大量的氯化镁,从海水中提取镁的生产流程如图所示: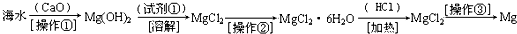
回答下列问题:
操作①主要是指______.试剂①可选用______,该反应的离子方程式为______.操作②是指______,经操作③最终可得金属镁,该反应的化学方程式是______.
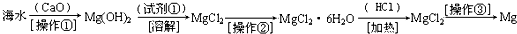
回答下列问题:
操作①主要是指______.试剂①可选用______,该反应的离子方程式为______.操作②是指______,经操作③最终可得金属镁,该反应的化学方程式是______.
氢氧化镁是难溶性的固体,将不溶性的固体和溶液分离的方法是过滤,氢氧化镁和盐酸反应生成氯化镁和水,离子方程式为:Mg(OH)2+2H+=Mg 2++2H2O,从溶液中析出固体采用蒸发结晶的方法,镁是活泼金属,在工业上采用电解氯化镁的方法冶炼镁,其电解反应方程式为:MgCl2
Mg+Cl2↑,
故答案为:过滤,盐酸,Mg(OH)2+2H+=Mg 2++2H2O,蒸发结晶,MgCl2
Mg+Cl2↑.
| ||
故答案为:过滤,盐酸,Mg(OH)2+2H+=Mg 2++2H2O,蒸发结晶,MgCl2
| ||

练习册系列答案
相关题目