题目内容
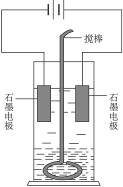
200 mL 2 mol·L-1的NaCl溶液(ρ="1.10" g·mL-1)在铜电极的电解池中不断搅拌下进行电解。当在阴极上有22.4 L的气体放出时停止电解。电解后溶液中NaCl的质量分数为( )
| A.12.72% | B.7.96% | C.8.30% | D.无法计算 |
A
这是一道重在考查考生审题能力、分析能力的题目,要求考生在审题时注意铜电极和惰性电极的差异。用铜电极电解NaCl溶液时,阳极反应式Cu-2e- Cu2+,阴极反应式:2H++2e-
Cu2+,阴极反应式:2H++2e- H2↑,电解总反应式:Cu+2H2O
H2↑,电解总反应式:Cu+2H2O Cu(OH)2↓+H2↑,可见,原NaCl溶液损失的仅仅是H2O。由反应式可知阴极上生成22.4 L H2时消耗的H2O为2 mol,即36 g。电解前m〔NaCl(aq)〕="1.10" g·mL-1×200 mL="220" g,电解后m〔NaCl(aq)〕="220" g-36 g="184" g,m(NaCl)="0.2" L×2 mol·L-1×58.5 g·mol-1="23.4" g。
Cu(OH)2↓+H2↑,可见,原NaCl溶液损失的仅仅是H2O。由反应式可知阴极上生成22.4 L H2时消耗的H2O为2 mol,即36 g。电解前m〔NaCl(aq)〕="1.10" g·mL-1×200 mL="220" g,电解后m〔NaCl(aq)〕="220" g-36 g="184" g,m(NaCl)="0.2" L×2 mol·L-1×58.5 g·mol-1="23.4" g。
w(NaCl)=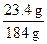 ×100%=12.72%。
×100%=12.72%。
 Cu2+,阴极反应式:2H++2e-
Cu2+,阴极反应式:2H++2e- H2↑,电解总反应式:Cu+2H2O
H2↑,电解总反应式:Cu+2H2O Cu(OH)2↓+H2↑,可见,原NaCl溶液损失的仅仅是H2O。由反应式可知阴极上生成22.4 L H2时消耗的H2O为2 mol,即36 g。电解前m〔NaCl(aq)〕="1.10" g·mL-1×200 mL="220" g,电解后m〔NaCl(aq)〕="220" g-36 g="184" g,m(NaCl)="0.2" L×2 mol·L-1×58.5 g·mol-1="23.4" g。
Cu(OH)2↓+H2↑,可见,原NaCl溶液损失的仅仅是H2O。由反应式可知阴极上生成22.4 L H2时消耗的H2O为2 mol,即36 g。电解前m〔NaCl(aq)〕="1.10" g·mL-1×200 mL="220" g,电解后m〔NaCl(aq)〕="220" g-36 g="184" g,m(NaCl)="0.2" L×2 mol·L-1×58.5 g·mol-1="23.4" g。w(NaCl)=
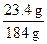 ×100%=12.72%。
×100%=12.72%。
练习册系列答案
相关题目