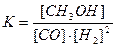题目内容
有如下两个反应:①E(g)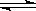 M(g)+N(g)②A(g)
M(g)+N(g)②A(g)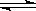 C(g)+B(g),起始时c(E)> c(A),且①的反应温度高于②(其他条件不变),则两反应的速率大小为:
C(g)+B(g),起始时c(E)> c(A),且①的反应温度高于②(其他条件不变),则两反应的速率大小为:
A.①>② B.①< ② C.①= ② D.无法确定
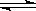 M(g)+N(g)②A(g)
M(g)+N(g)②A(g)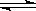 C(g)+B(g),起始时c(E)> c(A),且①的反应温度高于②(其他条件不变),则两反应的速率大小为:
C(g)+B(g),起始时c(E)> c(A),且①的反应温度高于②(其他条件不变),则两反应的速率大小为: A.①>② B.①< ② C.①= ② D.无法确定
D
分析:化学反应速率是整个过程的平均速率,温度会影响化学反应速率的快慢,反应温度和反应的吸放热情况有关.
解:化学反应速率是整个过程的平均速率,起始时c(E)>c(A),不能确定化学反应速率的大小,①的反应温度高于②,但是随后发生的化学反应的吸热和放热会引起化学反应中温度的变化,从而导致化学反应速率会发生变化,从另一个角度说,一般比较两个不同的化学反应中的速率意义不大,没有实际意义.
故选D.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 [来源:
[来源: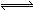 2Z(g)达到平衡,以Y的浓度改变表示的化学反应速率
2Z(g)达到平衡,以Y的浓度改变表示的化学反应速率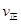 、
、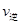 与时间的关系如下图,则Y的平衡浓度的表达式正确的是(式中S指对应区域的面积)( )
与时间的关系如下图,则Y的平衡浓度的表达式正确的是(式中S指对应区域的面积)( )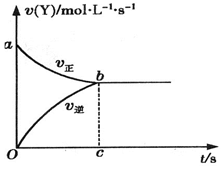
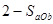
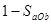
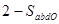
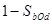
 cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示: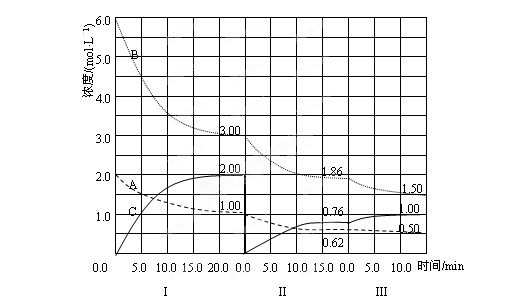
 的方向是_________,采取的措施是________;
的方向是_________,采取的措施是________; 和第Ⅲ阶段反应温度(T3)的高低:T2 T3(填“>”“<”“=”),判断的理由是_________________________________________;
和第Ⅲ阶段反应温度(T3)的高低:T2 T3(填“>”“<”“=”),判断的理由是_________________________________________;  随时间变化的趋势(曲线上必须标出A、B、C)。
随时间变化的趋势(曲线上必须标出A、B、C)。
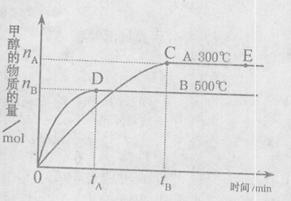
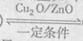 CH3OH (g)
CH3OH (g)