题目内容
在20mL 0.0025mol·L-1 AgNO3溶液中,加入5mL 0.01mol·L-1 KCl溶液,通过计算判断是否有AgCl沉淀生成。已知Ksp(AgCl)=1.8×10-10 (混合后溶液的总体积为两者体积之和)。
c(Ag+)×c(Cl-)>1.8×10-10,有AgCl沉淀生成。
试题分析:混合后溶液中的c(Ag+)=
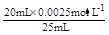 =0.0020mol·L-1 ,混合后溶液中的c(Cl-)=
=0.0020mol·L-1 ,混合后溶液中的c(Cl-)=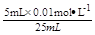 =0.0020mol·L-1 ,Qc = c(Ag+)×c(Cl-)=0.0020×0.0020=1×10-6 >1.8×10-10,根据溶度积规则判断。有AgCl沉淀生成。
=0.0020mol·L-1 ,Qc = c(Ag+)×c(Cl-)=0.0020×0.0020=1×10-6 >1.8×10-10,根据溶度积规则判断。有AgCl沉淀生成。
练习册系列答案
相关题目


 LaNi5+6Ni(OH)2。该电池放电时,负极反应是 。
LaNi5+6Ni(OH)2。该电池放电时,负极反应是 。