题目内容
11P+15CuSO4+24H2O====5Cu3P+6H3PO4+15H2SO4反应中,1 mol Cu2+能氧化P的物质的量是( )
| A.2/5 mol | B.11/5 mol | C.1/5 mol | D.1/3 mol |
C
氧化还原反应中氧化剂和还原剂得失电子数必相等,1 mol Cu2+氧化P的量也必须保证得失电子数相等。但15 mol CuSO4不是氧化11 mol P,因为P本身本有作氧化剂的。设1 mol Cu2+氧化P的物质的量为n,依得失电子数相等:
1 mol×1=n×5 n=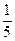 mol
mol
1 mol×1=n×5 n=
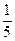 mol
mol
练习册系列答案
相关题目