��Ŀ����
ij��A����Է�������Ϊ84���ش��������⣺
��1����A�ķ���ʽΪ ��
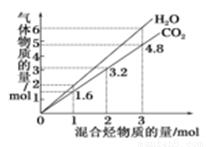
��2������������A�����������ϣ��������ʵ���һ�������ȼ��������������������� ����������һ�������ȼ��������������������� ��
A�� C7H8 B��C6H14 C��C7H14 D��C8H8
C7H8 B��C6H14 C��C7H14 D��C8H8
��3������AΪ���������������е�̼ԭ����ͬһƽ���ϣ��÷��ӵ�һ��ȡ����ֻ��һ�֡�
�� A�Ľṹ��ʽΪ ����Ϊ ��
�� ����A��Br2��CCl4��Һ��Ӧ����B��д����A����B�Ļ�ѧ����ʽ�� ��
�� ��A��Ϊͬ���칹�壬������̼ԭ�Ӹ�����A��ͬ�������� �֣�������A��
��4����A����ʹ��ˮ��ɫ������һ�ȴ���ֻ��һ�֣���A�Ľṹ��ʽΪ ��
 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д��������ȣ�ClNO�����л��ϳ��е���Ҫ�Լ�����ҵ�Ͽ���NO��Cl2�ϳɣ��ش��������⣺
(1)һ�������£����������������ڴ����еĺ������������ʱ�������������ȣ��漰�Ȼ�ѧ����ʽ��ƽ�ⳣ�����±���
��� | �Ȼ�ѧ����ʽ | ƽ�ⳣ�� |
�� | 2NO2(g)+NaCl(s) | K1 |
�� | 4NO2(g)+2NaCl(s) | K2 |
�� | 2NO(g)+ Cl2(g) | K3 |
��H3=_________���æ�H1����H2��ʾ����K3=__________����K1��K2 ��ʾ��
(2)300��ʱ����һ�ܱ������з�����Ӧ��2ClNO(g)  2NO(g)+ Cl2(g)��������Ӧ���ʱ���ʽΪv��=k��cn(ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
2NO(g)+ Cl2(g)��������Ӧ���ʱ���ʽΪv��=k��cn(ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
��� | c(ClNO)/mol��L-1 | v��/mol��L-1��s-1 |
�� | 0.30 | 3.60��10-9 |
�� | 0.60 | 1.44��10-8 |
�� | 0.90 | 3.24��10-8 |
��n=________��k=___________���ﵽƽ�������Сѹǿ�����������ƽ����������_______�����������С�����䡱����
(3)25��ʱ�������Ϊ2L�Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��0.08mol NO��0.04mol Cl2������Ӧ��2NO(g)+Cl2(g)  2ClNO(g) ��H
2ClNO(g) ��H
������Ӧ��ʼ��ƽ��ʱ�¶���ͬ����÷�Ӧ������ѹǿ��p����ʱ�䣨t���ı仯��ͼ������a��ʾ����H________0���>������<����ȷ��������������������ͬ�����ı�ijһ����ʱ�������ѹǿ��p����ʱ�䣨t���ı仯��ͼ������b��ʾ����ı��������___________��

��ͼ���Ǽס���ͬѧ���������Ӧƽ�ⳣ���Ķ���ֵ��lgK�����¶ȵı仯��ϵ��������ȷ��������____����ס����ҡ�����mֵΪ_______________��