��Ŀ����
��ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ������Ҫ����Դ��
��ش��������⣺
��1��2C2H2��g��+5O2��g���T4CO2��g��+2H2O��H=-2599kJ?mol-1������Ȳ��ȼ����Ϊ
��2����Щ��Ӧ���еú�������Щ��Ӧ������ֱ�ӷ�������Щ��Ӧ�IJ�Ʒ�������и���Ӧ������������ⶨ��Ӧ����������ѣ���ʱ�����ø�˹���ɣ��Ϳ��Լ�ӵذ����ǵķ�Ӧ�ȼ����������֪
��CO��g��+1/2O2��g���TCO2��g����H1=-283.0kJ?mol-1
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
��C��s��+1/2O2��g���TCO��g����H=
��3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪�����������±���
��ӦN2+3H2�T2NH3 ��H=a kJ?mol-1���Ը��ݱ������м������ݹ���a ����ֵ
��4���������Simons�ȿ�ѧ�ҷ����˲���ʹ�����ѻ�Ϊ��Ϳ�ֱ������ȼ�ϵ�صķ������÷�������Һ��ȼ�ϵ�ص��ŵ㣬�ֿ˷���Һ�ⲻ�ױ���IJ��㣮��װ��Ϊ�ò�����Ϊ�缫������ǿ����Һ�У�һ���缫ͨ���������һ�缫ͨ�백���������ܷ�ӦΪ4NH3+3O2�T2N2+6H2O����д�������缫��Ӧʽ
��ش��������⣺
��1��2C2H2��g��+5O2��g���T4CO2��g��+2H2O��H=-2599kJ?mol-1������Ȳ��ȼ����Ϊ
1299.5kJ?mol-1
1299.5kJ?mol-1
����2����Щ��Ӧ���еú�������Щ��Ӧ������ֱ�ӷ�������Щ��Ӧ�IJ�Ʒ�������и���Ӧ������������ⶨ��Ӧ����������ѣ���ʱ�����ø�˹���ɣ��Ϳ��Լ�ӵذ����ǵķ�Ӧ�ȼ����������֪
��CO��g��+1/2O2��g���TCO2��g����H1=-283.0kJ?mol-1
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
��C��s��+1/2O2��g���TCO��g����H=
-110.5kJ?mol-1
-110.5kJ?mol-1
����3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪�����������±���
| ��ѧ�� | ���ܣ�kJ/mol�� | ��ѧ�� | ���ܣ�kJ/mol�� |
| N��N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 |
-93
-93
����4���������Simons�ȿ�ѧ�ҷ����˲���ʹ�����ѻ�Ϊ��Ϳ�ֱ������ȼ�ϵ�صķ������÷�������Һ��ȼ�ϵ�ص��ŵ㣬�ֿ˷���Һ�ⲻ�ױ���IJ��㣮��װ��Ϊ�ò�����Ϊ�缫������ǿ����Һ�У�һ���缫ͨ���������һ�缫ͨ�백���������ܷ�ӦΪ4NH3+3O2�T2N2+6H2O����д�������缫��Ӧʽ
2NH3+6OH--6e-=N2+6H2O
2NH3+6OH--6e-=N2+6H2O
����������1��1mol��ȼ����ȫȼ�������ȶ���������ų�������Ϊȼ���ȣ�����Ȼ�ѧ����ʽ���㣻
��2�����ݸ�˹���ɣ���Ӧ��-�ٿɵ�Ŀ���Ȼ�ѧ����ʽ����Ӧ��Ҳ������Ӧ�ļ��㣻
��3����Ӧ��=��Ӧ����ܼ���-��������ܼ��ܣ��ݴ˽��
��4����������������Ӧ�������ڸ����ŵ磬�������������ɵ�����ˮ��
��2�����ݸ�˹���ɣ���Ӧ��-�ٿɵ�Ŀ���Ȼ�ѧ����ʽ����Ӧ��Ҳ������Ӧ�ļ��㣻
��3����Ӧ��=��Ӧ����ܼ���-��������ܼ��ܣ��ݴ˽��
��4����������������Ӧ�������ڸ����ŵ磬�������������ɵ�����ˮ��
����⣺��1��1mol��ȼ����ȫȼ�������ȶ���������ų�������Ϊȼ���ȣ���2C2H2��g��+5O2��g���T4CO2��g��+2H2O��H=-2599kJ?mol-1��֪����Ȳ��ȼ����Ϊ
��2599kJ?mol-1=1299.5kJ?mol-1��
�ʴ�Ϊ��1299.5kJ?mol-1��
��2����֪����CO��g��+
O2��g���TCO2��g����H1=-283.0kJ?mol-1
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
����ݸ�˹���ɣ���Ӧ��-�ٵ�C��s��+
O2��g���TCO��g�������H=-393.5kJ?mol-1-��-283.0kJ?mol-1��=-110.5kJ?mol-1��
�ʴ�Ϊ��-110.5kJ?mol-1��
��3����Ӧ��=��Ӧ����ܼ���-��������ܼ��ܣ���ӦN2+3H2�T2NH3 �ġ�H=942kJ/mol+3��437kJ/mol-2��3��391kJ/mol=-93kJ/mol��
�ʴ�Ϊ��-93��
��4����������������Ӧ�������ڸ����ŵ磬�������������ɵ�����ˮ�������缫��ӦʽΪ2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ��2NH3+6OH--6e-=N2+6H2O��
| 1 |
| 2 |
�ʴ�Ϊ��1299.5kJ?mol-1��
��2����֪����CO��g��+
| 1 |
| 2 |
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
����ݸ�˹���ɣ���Ӧ��-�ٵ�C��s��+
| 1 |
| 2 |
�ʴ�Ϊ��-110.5kJ?mol-1��
��3����Ӧ��=��Ӧ����ܼ���-��������ܼ��ܣ���ӦN2+3H2�T2NH3 �ġ�H=942kJ/mol+3��437kJ/mol-2��3��391kJ/mol=-93kJ/mol��
�ʴ�Ϊ��-93��
��4����������������Ӧ�������ڸ����ŵ磬�������������ɵ�����ˮ�������缫��ӦʽΪ2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ��2NH3+6OH--6e-=N2+6H2O��
���������⿼�鷴Ӧ�ȵ��йؼ��㡢ԭ��ص缫��Ӧʽ��д�ȣ��ѶȲ���ע����ݸ�˹���ɼ��㷴Ӧ�ȣ����ⷴӦ������ܵĹ�ϵ��

��ϰ��ϵ�д�
�����Ŀ
��ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ������Ҫ����Դ����ش��������⣺
��1��2C2H2��g��+5O2��g��=4CO2��g��+2H2O��l����H=-2599kJ?mol-1������Ȳ��ȼ����Ϊ ��
��2����Щ��Ӧ���еú�������Щ��Ӧ������ֱ�ӷ�������Щ��Ӧ�IJ�Ʒ�������и���Ӧ������������ⶨ��Ӧ����������ѣ���ʱ�����ø�˹���ɣ��Ϳ��Լ�ӵذ����ǵķ�Ӧ�ȼ����������֪
��CO��g��+
O2��g���TCO2��g����H1=-283.0kJ?mol-1
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
��C��s��+
O2��g��=CO��g����H= ��
��3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪�������������
��ӦN2+3H2?2NH3��H=a kJ?mol-1���Ը��ݱ������м������ݹ���a= ��
��1��2C2H2��g��+5O2��g��=4CO2��g��+2H2O��l����H=-2599kJ?mol-1������Ȳ��ȼ����Ϊ
��2����Щ��Ӧ���еú�������Щ��Ӧ������ֱ�ӷ�������Щ��Ӧ�IJ�Ʒ�������и���Ӧ������������ⶨ��Ӧ����������ѣ���ʱ�����ø�˹���ɣ��Ϳ��Լ�ӵذ����ǵķ�Ӧ�ȼ����������֪
��CO��g��+
| 1 |
| 2 |
��C��s��+O2��g���TCO2��g����H2=-393.5kJ?mol-1
��C��s��+
| 1 |
| 2 |
��3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̣���֪�������������
| ��ѧ�� | ���ܣ�kJ/mol�� | ��ѧ�� | ���ܣ�kJ/mol�� |
| N��N | 942 | H-O | 460 |
| N-H | 391 | O=O | 499 |
| H-H | 437 |
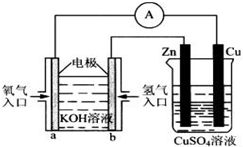 ����̼�����缫���������ˮ��Һ����Na2SO4��Һ ��AgNO3��Һ ��KCl��Һ ��CuCl2��Һ��ͨ����ͬ����ʱ�������������������ʵ�����ͬ���ǣ�����ţ�
����̼�����缫���������ˮ��Һ����Na2SO4��Һ ��AgNO3��Һ ��KCl��Һ ��CuCl2��Һ��ͨ����ͬ����ʱ�������������������ʵ�����ͬ���ǣ�����ţ� 2NH3 ��H��a kJ��mol��1���Ը��ݱ������м������ݹ���a����ֵ �� ��
2NH3 ��H��a kJ��mol��1���Ը��ݱ������м������ݹ���a����ֵ �� ��