题目内容
海水中溴常以NaBr形式存在,经分析海水中含溴0.07%,则海水中含NaBr的质量分数为_________________。从海水中提取溴的方法之一是:
①通入Cl2至浓缩的溴化物溶液,然后用空气把生成的溴吹出。
②Na2CO3溶液吸收溴(其中有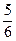 的溴的物质的量转化为Br-),同时放出CO2。
的溴的物质的量转化为Br-),同时放出CO2。
③向所得含溴化合物溶液中加稀H2SO4,溴又重新析出。
④得到的溴中可能夹杂少量的Cl2,再加入FeBr2除去。
第一步反应的离子方程式______________________________________________。
第二步反应的化学方程式______________________________________________。
第三步反应中氧化剂的化学式是________________________________________。
①通入Cl2至浓缩的溴化物溶液,然后用空气把生成的溴吹出。
②Na2CO3溶液吸收溴(其中有
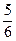 的溴的物质的量转化为Br-),同时放出CO2。
的溴的物质的量转化为Br-),同时放出CO2。③向所得含溴化合物溶液中加稀H2SO4,溴又重新析出。
④得到的溴中可能夹杂少量的Cl2,再加入FeBr2除去。
第一步反应的离子方程式______________________________________________。
第二步反应的化学方程式______________________________________________。
第三步反应中氧化剂的化学式是________________________________________。
0.09%
Cl2+2Br-====2Cl-+Br2
3Br2+3Na2CO3====5NaBr+NaBrO3+3CO2↑
NaBrO3
Cl2+2Br-====2Cl-+Br2
3Br2+3Na2CO3====5NaBr+NaBrO3+3CO2↑
NaBrO3
先计算100 g海水中NaBr的质量。
m(NaBr)="0.07" g×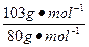 ="0.09" g
="0.09" g
海水中NaBr的质量分数为
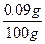 ×100%=0.09%
×100%=0.09%
m(NaBr)="0.07" g×
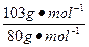 ="0.09" g
="0.09" g海水中NaBr的质量分数为
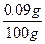 ×100%=0.09%
×100%=0.09%
练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目

 2SO3,催化剂一般是V2O5,下列对五氧化二钒作用的描述正确的是 。
2SO3,催化剂一般是V2O5,下列对五氧化二钒作用的描述正确的是 。
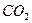 和
和