题目内容
【题目】过碳酸钠(2Na2CO3·3H2O2),有Na2CO3和H2O2的双重性质,用作漂白剂和氧化剂,可有效杀灭禽流感病毒。合理组合下列装置可用于测定过碳酸钠中碳酸钠的含量,下列说法不正确的是
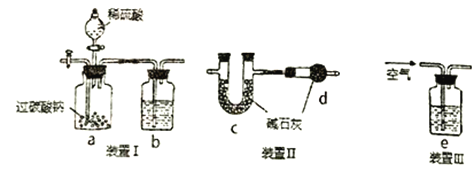
A. 装置皿→I→II的顺序连接装置
B. 装置b和e中盛放的试剂相同
C. d装置的作用是防止空气中的H2O和CO2进入到c中
D. 若b中盛放澄清的石灰水,只用装置I可验证过碳酸钠与硫酸反应是否生成CO2(不考虑空气CO2的影响)
【答案】B
【解析】A. 稀硫酸与过碳酸钠反应生成二氧化碳,由于空气中含有二氧化碳,所以利用空气排反应中产生的二氧化碳时需要除去空气中的二氧化碳,又因为还需要防止空气中的水蒸气进入c,所以连接顺序是装置皿→I→II,A正确;B. 装置b和e中盛放的试剂不相同,分别是浓硫酸和氢氧化钠溶液,B错误;C. d装置的作用是防止空气中的H2O和CO2进入到c中,C正确;D. 由于氢氧化钙溶液能吸收二氧化碳生成碳酸钙沉淀,因此若b中盛放澄清的石灰水,只用装置I可验证过碳酸钠与硫酸反应是否生成CO2(不考虑空气中CO2的影响),D正确,答案选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目