题目内容
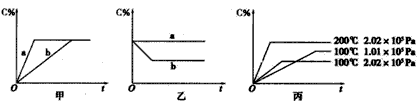
现有下列可逆反应:A(g)+B(g)=xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如图: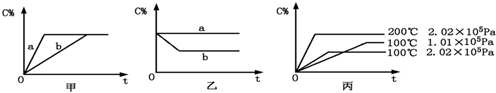
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则
(3)根据丙图可以判断该可逆反应的正反应是
(4)化学计量数x的值
分析:(1)使用催化剂,加快反应速率,缩短到达平衡的时间;
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动;
(4)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动.
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动;
(4)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动.
解答:解:(1)使用催化剂,加快反应速率,缩短到达平衡的时间,由图可知,a先到达平衡,故a曲线表示使用催化剂,b曲线表示没有使用催化剂,故答案为:b;
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动,C%不变,故答案为:a;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,正反应为吸热反应,
故答案为:吸;
(4)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,故x>1+1,即x>2,
故答案为:x>2;保持温度不变,增大压强,C%减小,说明平衡向逆反应方向移动,故x>1+1=2.
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动,C%不变,故答案为:a;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,正反应为吸热反应,
故答案为:吸;
(4)温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,故x>1+1,即x>2,
故答案为:x>2;保持温度不变,增大压强,C%减小,说明平衡向逆反应方向移动,故x>1+1=2.
点评:本题考查化学平衡图象、影响化学平衡的因素,难度中等,注意分析图象中曲线的变化特点,结合平衡移动原理解答.

练习册系列答案
相关题目
 2NH3(g) △H<0达到平衡的标志是__________________________(填编号)
2NH3(g) △H<0达到平衡的标志是__________________________(填编号) 2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是( )
2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是( ) xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图: