题目内容
在一定体积pH=1的HCl与HNO3的混合溶液中,逐滴加入c mol·L-1的AgNO3溶液,当溶液中的Cl-恰好完全沉淀时,溶液pH=2。若反应后溶液的体积等于反应前两溶液体积之和,则原溶液中NO3-的物质的量浓度是 ( )
| A.0.1c mol·L-1 | B.9c mol·L-1 |
| C.(0.1-9c) mol·L-1 | D.(0.9-c)mol·L-1 |
C
Cl-恰好完全沉淀时,反应后的溶液为硝酸,H+的物质的量不变。设原混合液的体积为V1,AgNO3溶液的体积为V2,由H+守恒得0.1V1=0.01(V1+V2)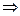 9V1=V2。再由混合液中NO3-、Cl-、H+的电荷守恒得出答案为C
9V1=V2。再由混合液中NO3-、Cl-、H+的电荷守恒得出答案为C
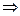 9V1=V2。再由混合液中NO3-、Cl-、H+的电荷守恒得出答案为C
9V1=V2。再由混合液中NO3-、Cl-、H+的电荷守恒得出答案为C
练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
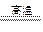 8Cu+4FeO+2Fe2O3+16SO2,下列有关说法不正确的是( )
8Cu+4FeO+2Fe2O3+16SO2,下列有关说法不正确的是( )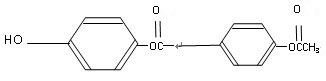 与足量的NaOH
与足量的NaOH