题目内容
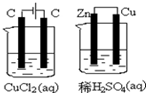 关于如图装置所示的两个实验,说法正确的是( )
关于如图装置所示的两个实验,说法正确的是( )分析:①是电解池②是原电池,①中阳极上氯离子放电生成氯气,阴极上铜离子放电生成铜,②中锌作负极,铜作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应,电流从正极沿导线流向负极,据此分析解答.
解答:解:A.①是电解池,是电能转化为化学能的装置,②是原电池,是化学能转化为电能的装置,故A错误;
B.②中电流的方向是从铜沿导线流向锌,故B错误;
C.反应开始阶段,①中阳极上析出氯气,阴极上析出铜,②中正极上生成氢气,负极上生成锌离子,故C错误;
D.阳极上失电子发生氧化反应,正极上得电子发生还原反应,其电极反应式:①中阳极 2Cl--2e→Cl2↑②中正极 2H++2e→H2↑,故D正确;
故选D.
B.②中电流的方向是从铜沿导线流向锌,故B错误;
C.反应开始阶段,①中阳极上析出氯气,阴极上析出铜,②中正极上生成氢气,负极上生成锌离子,故C错误;
D.阳极上失电子发生氧化反应,正极上得电子发生还原反应,其电极反应式:①中阳极 2Cl--2e→Cl2↑②中正极 2H++2e→H2↑,故D正确;
故选D.
点评:本题考查原电池和电解池原理,明确放电顺序及电流方向即可解答,注意原电池和电解池的区别.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
关于如图装置所示的两个实验,说法正确的是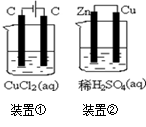
| A.两个装置中都发生了化学变化,都由化学能转变为电能 |
| B.装置②中电流方向是从Zn经导线流入Cu |
| C.反应开始阶段,两个装置中均有氢气产生 |
| D.电极反应式:阳极 2Cl—-2e-→Cl2↑正极 2H++2e-→H2↑ |
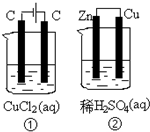 (2010?普陀区二模)关于如图装置所示的两个实验,说法正确的是( )
(2010?普陀区二模)关于如图装置所示的两个实验,说法正确的是( )
