题目内容
(1)向Ba(OH)2溶液中逐滴加入NaHSO4溶液至钡离子恰好沉淀完全,请写出发生反应的离子方程式: 。
(2)在以上溶液中,继续滴加NaHSO4溶液,请写出此步反应的离子方程式: 。
(2)在以上溶液中,继续滴加NaHSO4溶液,请写出此步反应的离子方程式: 。
Ba2++OH-+H++SO42-=BaSO4↓+H2O;H++OH-=H2O。
本题实际上是上述例题的变式,假设Ba(OH)2的物质的量为1mol,则只须NaHSO4即可把其中的钡离子沉淀完全,参加反应的Ba2+、OH-、H+、SO42-物质的量比为1∶1∶1∶1,此时,剩余1mol OH-,如继续滴加NaHSO4溶液,则只是OH-与H+的中和反应。

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
 +Ba2++OH-====BaSO4↓+H2O
+Ba2++OH-====BaSO4↓+H2O +2H
+2H
 CO
CO ↑+H
↑+H
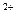 +2OH
+2OH
 ↓_____________________________。
↓_____________________________。 Cl2↑+ Mn2+ + H2O
Cl2↑+ Mn2+ + H2O