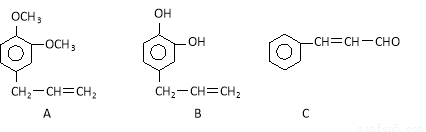
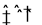题目内容
pH=2的两种一元酸X和Y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示.分别滴加0.1 mol/L NaOH至pH=7,消耗NaOH溶液的体积为Vx、Vy,下列说法正确的是

A.X为弱酸,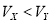 B.Y为强酸,
B.Y为强酸,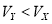
C.X为强酸,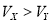 D.Y为弱酸,
D.Y为弱酸,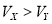
B
【解析】
试题分析:本题考查强酸和弱酸的电离,根据酸稀释pH的变化判断强酸、弱酸是解题的关键。分析题给图像知,稀释10倍,x的pH值变化1,y的pH值变化小于1,弱酸存在电离平衡,稀释促进电离,PH变化小,说明x为弱酸,y为强酸;强酸全部电离,而弱酸部分电离,pH相等的强酸和弱酸,弱酸的物质的量浓度大,体积均为100 mL的X和Y与浓度均为0.1 mol/LNaOH溶液反应,弱酸消耗碱的量大,即Vy<Vx,选B。
考点:考查强弱电解质的对比及浓度对电离平衡的影响。

练习册系列答案
相关题目