题目内容
(15分)用下图装置进行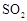 转化为
转化为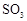 的转化率测定实验:
的转化率测定实验:

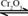
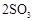 ;
;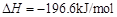 。已知:
。已知:
|
|
熔点( |
沸点( |
|
|
-72.4 |
-10 |
|
|
16.8 |
44.3 |
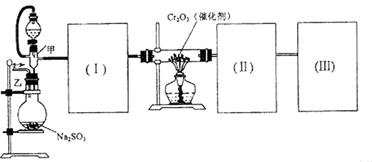
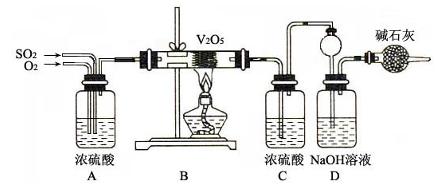
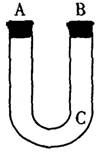
(1)要顺利进行实验,上图Ⅰ、Ⅱ、Ⅲ处各应连接合适的装置(可重复使用),请从下列A~E中选择适宜的装置,将其序号填入空格内。

(2)将装置连接好,实验前,必须进行的操作是(不必写具体过程) 。
(3)实验时,浓硫酸能顺利滴入烧瓶中,甲装置所起的作用是 。
(4)开始实验时,先从乙处均匀通入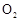 ,为使
,为使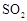 有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是
。
有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是
。
(5)实验中“当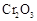 表面红热时,应将酒精灯移开一会儿再加热”,以防温度过高,这样做的原因是
;若用大火加热有
表面红热时,应将酒精灯移开一会儿再加热”,以防温度过高,这样做的原因是
;若用大火加热有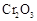 处的反应管时,
处的反应管时,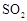 的转化率会
(填“升高”、“降低”或“不变”)。
的转化率会
(填“升高”、“降低”或“不变”)。
(6)实验时若用25.2g的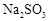 ,加入的浓硫酸是足量的,反应结束时继续通入
,加入的浓硫酸是足量的,反应结束时继续通入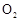 一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中
一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中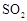 的转化率为
%(保留小数点后一位)。
的转化率为
%(保留小数点后一位)。
(1)`Ⅰ:B Ⅱ:A Ⅲ:BE(各1分,共3分)
(2)检查装置的气密性(2分)
(3)保持分液漏斗内压强与烧瓶内压强相等(2分)
(4)先加热催化剂,然后缓慢滴加浓硫酸(2分)
(5)温度过高不利于SO3的生成,且影响催化剂的活性(2分) 降低(2分)
(6)70.6%(2分)
【解析】综合题给信息,实验装置自左至右分别为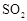 的发生装置生成
的发生装置生成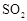 ,经浓硫酸干燥(I)后催化氧化,生成的SO3的经冰水冷凝(II)在U型管中,为了避免SO3吸水及SO2污染空气,在(III)中填加浓硫酸的吸水装置及NaOH的尾气吸收装置。
,经浓硫酸干燥(I)后催化氧化,生成的SO3的经冰水冷凝(II)在U型管中,为了避免SO3吸水及SO2污染空气,在(III)中填加浓硫酸的吸水装置及NaOH的尾气吸收装置。
(4)为防止SO2的损失应该先预热催化剂,然后缓慢滴加浓硫酸
(5)2SO2+O2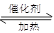 2SO3,正反应是放热反应,温度过高不利于SO3的生成,且影响催化剂的活性。
2SO3,正反应是放热反应,温度过高不利于SO3的生成,且影响催化剂的活性。
(6)Na2SO3 → SO2 → SO3
可: 25.2g 16g
故:SO2的转化率为:11.3/16 = 70.6%

 考前必练系列答案
考前必练系列答案 )
)