题目内容
可逆反应:2A(气)+3B(气) 3C(气),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是( )
3C(气),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是( )A.各物质的浓度之比为c(A):c(B):c(C)=2:3:3
B.气体的总体积是反应开始时的
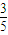
C.混合气体的密度不变
D.单位时间内,若消耗了amolA物质,同时也消耗了1.5amol的C物质
【答案】分析:可逆反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的物理量不变,注意本题中气体反应物的化学计量数之和大于气体生成物的化学计量数之和的特征.
解答:解:A.平衡时各物质的浓度之比取决于起始配料比以及转化的程度,不能作为判断是否达到平衡状态的依据,故A错误;
B.反应为可逆反应,不可能完全转化,则气体的总体积不可能为反应开始时的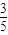 ,故B错误;
,故B错误;
C.由于气体的总质量不变,容器的体积不变,则无论是否达到平衡状态,气体的密度都不变,则不能作为判断是否达到平衡状态的依据,故C错误;
D.单位时间内,若消耗了amolA物质,同时也消耗了1.5amol的C物质,说明正逆反应速率相等,达到平衡状态,故D正确.
故选D.
点评:本题考查化学平衡状态的判断,题目难度不大,答题时注意化学反应气体的化学计量数关系,此为解答该题的关键.
解答:解:A.平衡时各物质的浓度之比取决于起始配料比以及转化的程度,不能作为判断是否达到平衡状态的依据,故A错误;
B.反应为可逆反应,不可能完全转化,则气体的总体积不可能为反应开始时的
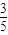 ,故B错误;
,故B错误;C.由于气体的总质量不变,容器的体积不变,则无论是否达到平衡状态,气体的密度都不变,则不能作为判断是否达到平衡状态的依据,故C错误;
D.单位时间内,若消耗了amolA物质,同时也消耗了1.5amol的C物质,说明正逆反应速率相等,达到平衡状态,故D正确.
故选D.
点评:本题考查化学平衡状态的判断,题目难度不大,答题时注意化学反应气体的化学计量数关系,此为解答该题的关键.

练习册系列答案
相关题目
现有可逆反应:2A(g)+2B(g)?C(g)+3D(g),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
| A、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同 | B、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的平均相对分子质量相同 | C、达到平衡时,Ⅰ途径A的平衡浓度等于Ⅱ途径A的平衡浓度 | D、达到平衡时,Ⅰ途径所得混合气密度为Ⅱ途径所得混合气密度的2倍 |
 3C(气),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是( )
3C(气),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是( )
