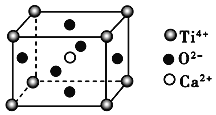
��Ŀ����
����Ŀ����������������������Ź㷺����;����ش��������⡣
(1)Fe2+��M������Ų�ʽ____________��Ԫ��Fe��Mn�ĵ��������ֱܷ�ΪI3(Fe)��I3(Mn)����I3(Fe)______I3(Mn)(����>������<")��
(2)���������У���Alԭ��δ�ɶԵ�������ͬ�Ľ���Ԫ����_______�֡���̬�Ȼ����ķ������Ϊ(AlCl3)2������Al��Cl����8e-�ȶ��ṹ��Alԭ�ӵ��ӻ���ʽΪ_________�����ݵȵ���ԭ����AlO2���Ŀռ乹��Ϊ____________����ѧʵ��֤����ͨ��״̬�²�������NaAlO2 �� Al(OH)3����ǿ����Һ�γɵ������ӣ�ʵ������ΪAl(OH)3��������ԭ������������δ�ﵽ���� ������OH�������γ���λ����Al(OH)3��Ӧʱֻ���к�1molOH��,����ΪһԪ�ᣬд��Al(OH)3�������Եĵ���ķ���ʽ______________��
(3)Fe(CO)5���۵�Ϊ-20�棬�е�Ϊ103�棬���������ѣ���Fe(CO)5�����Ļ��ϼ�Ϊ_______����Fe(CO)5����������������Ŀ֮��Ϊ______����
(4)��λ������K3[Fe(CN)n]���������ӻ������ɫ��������˿����ڼ����������ӣ���֪��ԭ�ӵ������������������ṩ������֮��Ϊ14����n=_____����������ɫ�����Ļ�ѧʽ____________��
���𰸡�3s23p63d6 < 4 sp3 ֱ���� Al(OH)3 + H2O ![]() [Al(OH)4]��+ H+ 0 1:1 6 Fe3 [Fe(CN)6]2
[Al(OH)4]��+ H+ 0 1:1 6 Fe3 [Fe(CN)6]2
��������
��1��Fe��ԭ������Ϊ26����̬Fe2+�ĵ���Ϊ24����Mn2+ת��ΪMn3+ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬תΪ���ȶ���3d4״̬����Fe2+��Fe3+ʱ��3d�ܼ��ɲ��ȶ���3d6���ȶ���3d5�����״̬��
��2��Alԭ��δ�ɶԵ�����Ϊ1����AlCl3��2��������������4����λ�������ӳɼ�������3��Ϊ���ۼ���һ��Ϊ��λ������AlO2����CO2��ԭ�Ӹ�����Ϊ3,�۵�������Ϊ16����Ϊ�ȵ����壻��������������ʽ����ʱ����ˮ��������������γ���λ�������[Al(OH)4]����ʹ��Һ�����ԣ�
��3��Fe��CO��5����Ԫ�صĻ��ϼ�Ϊ0�ۣ�Fe(CO)5��CO����ԭ��֮����5��������ÿ��CO��������1��������2��������
��4������λ������K3[Fe��CN��n]��ÿ����������ṩһ�Ե��ӣ�����ԭ���������2�����ӣ�����ԭ�ӵ������������������ṩ������֮��Ϊ14���ɵ�2+2n=14��
��1��Fe��ԭ������Ϊ26����̬Fe2+�ĵ���Ϊ24��������Ų�ʽΪ1s22s22p63s23p63d6����Mn2+ת��ΪMn3+ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬תΪ���ȶ���3d4״̬��Ҫ�������϶ࣻ��Fe2+��Fe3+ʱ��3d�ܼ��ɲ��ȶ���3d6���ȶ���3d5�����״̬����Ҫ���������Ҫ�٣��ʴ�Ϊ��3s23p63d6��<��
��2��Alԭ��δ�ɶԵ�����Ϊ1���������ڸ�����Ԫ���У�δ�ɶԵ�����ҲΪ1����K��Sc��Cu��Ga������4�֣���̬�Ȼ������Ϊ�����壨AlCl3��2������Al��Cl����8e-�ȶ��ṹ��˵����������������4����λ�������ӳɼ�������3��Ϊ���ۼ���һ��Ϊ��λ����Alԭ�ӵ��ӻ���ʽΪsp3�ӻ���AlO2����CO2��ԭ�Ӹ�����Ϊ3,�۵�������Ϊ16����Ϊ�ȵ����壬CO2�Ŀռ乹��Ϊֱ���Σ���AlO2���Ŀռ乹��Ϊֱ���Σ���Al(OH)3��������ԭ������������δ�ﵽ���� ������OH�������γ���λ����Al(OH)3��Ӧʱֻ���к�1molOH��������ΪһԪ���֪����������������ʽ����ʱ����ˮ��������������γ���λ�������[Al(OH)4]����ʹ��Һ�����ԣ����뷽��ʽΪAl(OH)3 + H2O ![]() [Al(OH)4]��+ H+���ʴ�Ϊ��4��sp3�ӻ���ֱ���Σ�Al(OH)3 + H2O
[Al(OH)4]��+ H+���ʴ�Ϊ��4��sp3�ӻ���ֱ���Σ�Al(OH)3 + H2O ![]() [Al(OH)4]��+ H+��
[Al(OH)4]��+ H+��
��3��Fe��CO��5����Ԫ�صĻ��ϼ�Ϊ0�ۣ�Fe(CO)5��CO����ԭ��֮����5��������ÿ��CO��������1��������2��������Fe(CO)5������Ϊ10��,����Ϊ10����������������Ŀ֮��Ϊ1:1���ʴ�Ϊ��0��1:1��
��4������λ������K3[Fe��CN��n]��ÿ����������ṩһ�Ե��ӣ�����ԭ���������2�����ӣ�����ԭ�ӵ������������������ṩ������֮��Ϊ14���ɵ�2+2n=14������n=6��K3[Fe��CN��6]���������ӷ�Ӧ����Fe3 [Fe(CN)6]2��ɫ�������ʴ�Ϊ��6��Fe3[Fe(CN)6]2��