题目内容
由人尿分离出来的结晶化合物A,熔点为187~188 ℃。对化合物A做下列实验:
(1)测得A的蒸气密度为8.000 g·L-1(已折合成标准状况),取17.92 g A完全燃烧,生成的气体通过浓硫酸,浓硫酸增重8.100 g。剩余气体通过碱石灰,气体质量减轻39.60 g;另取17.92 gA完全分解,可得标准状况下氮气1.120L,试通过计算确定A的化学式。
(2)又知A和足量6 mol·L-1的盐酸混合加热可以完全水解,1 molA水解生成1 mol B和1 mol C。已知A、B、C三物质分子中均含有一个羧基;B物质仅由碳、氢、氧三种元素组成,其物质的量之比为7∶6∶2;C俗名为甘氨酸。写出A、B、C的结构简式。A__________,B__________,C__________。
(1)C9H9NO3
(2)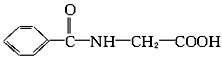
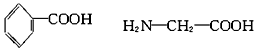
解析:
(1)MA=8.000 g·L-1×22.4 L· mol-1=179.2 g· mol-1,则17.92g A的物质的量为0.100 0 mol,完全燃烧生成水的物质的量为:![]() 生成CO2的物质的量为:
生成CO2的物质的量为:![]() 生成N2的物质的量为:
生成N2的物质的量为:![]() 则n(A)∶n(C)∶n(H)∶n(N)∶n(O)=1∶9∶9∶1∶3,则A的化学式为C9H9NO3。
则n(A)∶n(C)∶n(H)∶n(N)∶n(O)=1∶9∶9∶1∶3,则A的化学式为C9H9NO3。
(2)B的化学式为C7H6O2,分子中含一个羧基,则其结构简式为:![]() ,C为甘氨酸,其结构简式为:H2N—CH2—COOH,A的结构简式为:
,C为甘氨酸,其结构简式为:H2N—CH2—COOH,A的结构简式为:
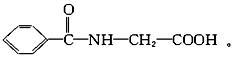

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目