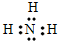题目内容
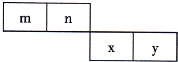 m、n、x、y四种主族元素在周期表的相对位置如图所示,已知它的原子序数之和为46,请回答:
m、n、x、y四种主族元素在周期表的相对位置如图所示,已知它的原子序数之和为46,请回答:(1)m与Y所形成化合物属
(2)x原子的结构示意图
(3)n与y的氢化物相互作用生成物质的电子式
分析:m、n、x、y四种主族元素在周期表的相对位置如图所示,已知它的原子序数之和为46,设m的原子序数为z,则n的原子序数为z+1,x的原子序数为z+10,y的原子序数为z+11,则有z+z+1+z+10+z+11=46,z=6,所以m为C元素,n为N元素,x为S元素,y为Cl元素,然后根据元素对应的单质及其化合物的性质解答该题.
解答:解:m、n、x、y四种主族元素在周期表的相对位置如图所示,已知它的原子序数之和为46,设m的原子序数为z,则n的原子序数为z+1,x的原子序数为z+10,y的原子序数为z+11,则有z+z+1+z+10+z+11=46,z=6,所以m为C元素,n为N元素,x为S元素,y为Cl元素,
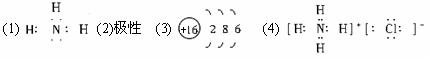
(1)m与Y所形成化合物为CCl4,存在C-Cl极性键,为正四面体结构,正负电荷中心重合,为非极性分子,故答案为:极性;非极性;
(2)S的原子序数为16,原子结构示意图为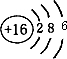 ,m与x形成化合物的结构式为S=C=S,故答案为:
,m与x形成化合物的结构式为S=C=S,故答案为: ;S=C=S;
;S=C=S;
(3)n与y的氢化物相互作用生成物质为NH4Cl,其电子式为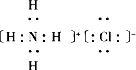 ,故答案为:
,故答案为: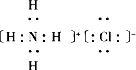 .
.
(1)m与Y所形成化合物为CCl4,存在C-Cl极性键,为正四面体结构,正负电荷中心重合,为非极性分子,故答案为:极性;非极性;
(2)S的原子序数为16,原子结构示意图为
 ,m与x形成化合物的结构式为S=C=S,故答案为:
,m与x形成化合物的结构式为S=C=S,故答案为: ;S=C=S;
;S=C=S;(3)n与y的氢化物相互作用生成物质为NH4Cl,其电子式为
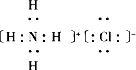 ,故答案为:
,故答案为: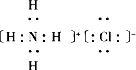 .
.点评:本题考查元素的推断以及对应单质、化合物的性质,题目难度不大,解答本题时注意从元素在周期表中的相对位置判断质子数之间的关系.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
 M、N、X、Y四种主族元素在周期表里的相对位置如图所示,已知它们的原子序数总和为46.
M、N、X、Y四种主族元素在周期表里的相对位置如图所示,已知它们的原子序数总和为46.
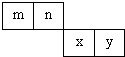 m、n、x、y 四种主族元素在周期表里的相对位置如图所示.已知它们的原子序数总和为46,则:
m、n、x、y 四种主族元素在周期表里的相对位置如图所示.已知它们的原子序数总和为46,则: