题目内容
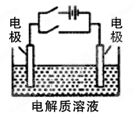
如图为用酸性氢氧燃料电池为电源进行电解的实验装置示意图。下列说法中,正确的是
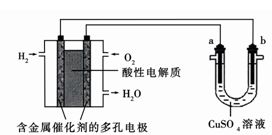

| A.燃料电池工作时,正极反应为:O2 + 4H++ 4e-= 2H2O |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是含锌、铁的粗铜,b极是纯铜, a极溶解铜的质量与b极析出铜的质量相等 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
A
试题分析:A、酸性条件下,正极发生的反应为:O2 + 4H++ 4e-= 2H2O,正确; B、a极是铁,b极是铜时,a极逐渐溶解, b极上有铜析出,错误;C、a极是含锌、铁的粗铜,b极是纯铜,工作时,a极的锌先溶解,当锌溶解完之后,铜才溶解,而在b极上析出的全是铜,因此a极溶解铜的质量与b极析出铜的质量不相等,错误;D、a、b两极均是石墨时,在相同条件下a极发生的电极反应是:4OH――4e-=O2↑+2H2O,而在电池中消耗的是氢气,肯定不相等。

练习册系列答案
相关题目
 NiOOH+1/2H2,充电时阴极反应为:H2O+e-===1/2H2↑+OH-。则下列说法正确的是(双选) ( )。
NiOOH+1/2H2,充电时阴极反应为:H2O+e-===1/2H2↑+OH-。则下列说法正确的是(双选) ( )。
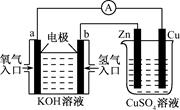
 3Zn(OH)2+2Fe(OH)3+4KOH,按要求回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH,按要求回答下列问题: