题目内容
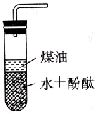
往如图所示的试管中投入一块金属钠,可观察到钠首先沉到煤油底部,一接触到水层就产生大量气泡,使钠块变成球状并向上浮,同时水层变红色,过一会儿,钠又慢慢沉降到两种液体的交界处,一接触到水层,又立即产生大量气泡,使钠上浮,如此反复多次,直至钠反应完为止,回答下列问题.
上述现象说明钠的物理性质有______,说明钠的化学性质是______(用化学方程式表示).
上述现象说明钠的物理性质有______,说明钠的化学性质是______(用化学方程式表示).

管中投入一块金属钠,可观察到钠首先沉到煤油底部,说明钠的密度比煤油大,一接触到水层就产生大量气泡,使钠块变成球状并向上浮,密度小于小,同时水层变红色,说明有碱性物质生成,有气体产生,证明金属钠和水之间反应产物是氢氧化钠和氢气,故答案为:钠的密度比水小,比煤油大,钠的熔点比较低;2Na+2H2O═2NaOH+H2↑.

练习册系列答案
相关题目