题目内容
下列有关实验说法不正确的是( )
| A.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
| B.向少量的火柴头浸泡液中滴加AgNO3、稀HNO3和NaNO2,检验火柴头中的氯元素 |
| C.制备摩尔盐时,最后在蒸发皿中蒸发浓缩溶液,加热至液体表面出现晶膜为止,不能将溶液全部蒸干 |
| D.检验氯乙烷中的氯元素时,将氯乙烷和NaOH溶液混合加热后,用稀硫酸进行酸化 |
A.电化学反应较化学反应快,锌和铁在酸性条件下可形成原电池反应,反应速率较快,可用于判断,故A正确;
B.火柴头中含有KClO3,检验氯元素,应把ClO3-还原为4Cl-,酸性条件下,NO2-具有还原性,向少量的火柴头浸泡液中滴加AgNO3、稀HNO3和NaNO2,发生的离子反应为:ClO3-+3NO2-+Ag+═AgCl↓+3NO3-,出现白色沉淀,证明含有氯元素,故B正确;
C.将蒸发皿置于水浴上蒸发、浓缩至表面出现结晶薄膜为止,放置冷却,得(NH4)2SO4?FeSO4?6H2O晶体,不能将溶液全部蒸干,以防温度过高导致(NH4)2SO4?FeSO4?6H2O分解,故C正确;
D.用稀硫酸进行酸化,可生成微溶于水的硫酸银沉淀,影响实验结论,应用硝酸酸化,故D错误.
故选D.
B.火柴头中含有KClO3,检验氯元素,应把ClO3-还原为4Cl-,酸性条件下,NO2-具有还原性,向少量的火柴头浸泡液中滴加AgNO3、稀HNO3和NaNO2,发生的离子反应为:ClO3-+3NO2-+Ag+═AgCl↓+3NO3-,出现白色沉淀,证明含有氯元素,故B正确;
C.将蒸发皿置于水浴上蒸发、浓缩至表面出现结晶薄膜为止,放置冷却,得(NH4)2SO4?FeSO4?6H2O晶体,不能将溶液全部蒸干,以防温度过高导致(NH4)2SO4?FeSO4?6H2O分解,故C正确;
D.用稀硫酸进行酸化,可生成微溶于水的硫酸银沉淀,影响实验结论,应用硝酸酸化,故D错误.
故选D.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
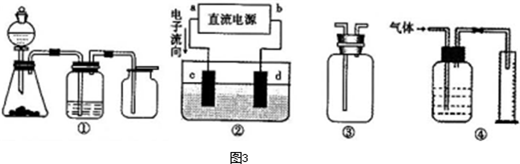
某课外活动小组进行电解饱和食盐水的实验(如图)。请同答下列问题。
(1)通电一段时间后,可观察到_______________电极(填
“阴极”或“阳极”)附近溶液颜色先变红,该电极上的电
极反应式为____________。
(2)该溶液电解反应的化学方程式为 。
(3)若开始时改用铁棒做阳极,阳极的电极反应式为 ___________________________________。
(4)若用H2和O2为反应物,以KOH为电解质溶液,可构成新型燃料电池(如下图),两个电极均由多孔性炭制成,通入的气体由孔隙中逸出,并在电极表面放电。其中a是___极(填“正”或“负”),b极的电极反应式为 。
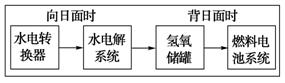
(5)下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是 (填序号)
| A.该能量转化系统中的水也是可以循环的 |
| B.燃料电池系统产生的能量实际上来自于水 |
| C.燃料电池放电时的正极反应: H2-2e-+2OH-=2H2O |
| D.水电解系统中的阳极反应:4OH-―4e-=2H2O+O2↑ |