题目内容
【题目】硅在地壳中的含量较高.硅及其化合物的开发由来已久,在现代生活中有广泛应用.回答下列问题:
(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”.这种“金属”可能是 .
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料.其中,生产普通玻璃的主要原料有 .
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料.工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下: 
发生的主要反应 | |
电弧炉 | SiO2+2C |
流化床反器 | Si+3HCl |
还原炉 | SiHCl3+H2 |
①用石英砂和焦炭在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为;碳化硅又称 , 其晶体结构与相似.
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和 .
物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | ﹣30.4 | ﹣84.9 | ﹣111.9 |
③SiHCl3极易水解,其完全水解的产物为 .
(4)氯碱工业可为上述工艺生产提供部分原料,这些原料是 .
【答案】
(1)含有硅碳的铁合金
(2)纯碱、石英和石灰石
(3)SiO2+3C ![]() SiC+2CO↑;金刚砂;金刚石;精馏(或蒸馏);H4SiO4(或H2SiO3)、H2、HCl
SiC+2CO↑;金刚砂;金刚石;精馏(或蒸馏);H4SiO4(或H2SiO3)、H2、HCl
(4)H2、HCl
【解析】解:(1)石英砂的主要成分是二氧化硅,加热石英砂、木炭和铁时,发生置换反应,SiO2+2C ![]() Si+2CO↑,所以在加热石英砂、木炭和铁时,得到一种“金属”.这种“金属”可能是含有硅碳的铁合金, 所以答案是:含有硅碳的铁合金;(2)制造普通玻璃的主要原料是:纯碱、石灰石和石英,在玻璃窑中强热时的主要发生反应:SiO2+Na2CO3
Si+2CO↑,所以在加热石英砂、木炭和铁时,得到一种“金属”.这种“金属”可能是含有硅碳的铁合金, 所以答案是:含有硅碳的铁合金;(2)制造普通玻璃的主要原料是:纯碱、石灰石和石英,在玻璃窑中强热时的主要发生反应:SiO2+Na2CO3 ![]() Na2SiO3+CO2↑、SiO2+CaCO3
Na2SiO3+CO2↑、SiO2+CaCO3 ![]() CaSiO3+CO2↑,所以答案是:纯碱、石英和石灰石;(3)①石英砂的主要成分是二氧化硅,在反应中生成碳化硅,反应为:SiO2+3C
CaSiO3+CO2↑,所以答案是:纯碱、石英和石灰石;(3)①石英砂的主要成分是二氧化硅,在反应中生成碳化硅,反应为:SiO2+3C ![]() SiC+2CO↑,碳化硅又称金刚砂,其晶体结构与金刚石相似,所以答案是:SiO2+3C
SiC+2CO↑,碳化硅又称金刚砂,其晶体结构与金刚石相似,所以答案是:SiO2+3C ![]() SiC+2CO↑;金刚砂;金刚石;②利用沸点的不同提纯SiHCl3属于蒸馏,SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点﹣84.7℃),由于沸点差别较大,可以通过精馏(或蒸馏)除去杂质,所以答案是:精馏(或蒸馏);③SiHCl3水解反应方程式为:SiHCl3+3H2O═H2SiO3+H2↑+3HCl↑,生成硅酸、氢气和氯化氢,所以答案是:H4SiO4(或H2SiO3)、H2、HCl;(4)氯碱工业主要反应为电解饱和食盐水:2NaCl+2H2O
SiC+2CO↑;金刚砂;金刚石;②利用沸点的不同提纯SiHCl3属于蒸馏,SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点﹣84.7℃),由于沸点差别较大,可以通过精馏(或蒸馏)除去杂质,所以答案是:精馏(或蒸馏);③SiHCl3水解反应方程式为:SiHCl3+3H2O═H2SiO3+H2↑+3HCl↑,生成硅酸、氢气和氯化氢,所以答案是:H4SiO4(或H2SiO3)、H2、HCl;(4)氯碱工业主要反应为电解饱和食盐水:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,为该化学工艺提供H2、HCl,所以答案是:H2、HCl.
2NaOH+H2↑+Cl2↑,为该化学工艺提供H2、HCl,所以答案是:H2、HCl.

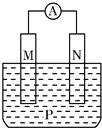
【题目】如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是( )
M | N | P | |
A | Zn | Cu | 稀H2SO4溶液 |
B | Cu | Fe | 稀HCl溶液 |
C | Ag | Zn | AgNO3溶液 |
D | Zn | Fe | Fe(NO3)3溶液 |
A.A
B.B
C.C
D.D

