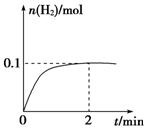
题目内容
H2(g)+I2(g)![]() 2HI(g);△H<0可逆反应已达化学平衡,下列图象中正确的是( )
2HI(g);△H<0可逆反应已达化学平衡,下列图象中正确的是( )
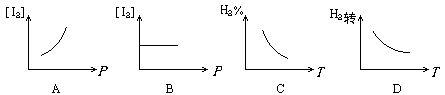
BD
解析:
结合反应的特点,增大压强,平衡不移动,[I2]不变;升高温度,平衡向逆反应方向移动,H2%增大,H2的转化率减小。

练习册系列答案
相关题目
|
一定温度下,在一个容积为1 L的密闭容器中,充入1 mol H2(g)和1 mol I2(g),发生反应H2(g)+I2(g) | |
| [ ] | |
A. |
后一反应的平衡常数为1 |
B. |
后一反应的平衡常数为0.5 |
C. |
后一反应达到平衡时,H2的平衡浓度为0.25 mol·L-1 |
D. |
后一反应达到平衡时,HI(g)的平衡浓度为0.5 mol·L-1 |
已知450℃时,反应H2(g)+I2(g)  2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g)  H2(g)+I2(g)的化学平衡常 数为
H2(g)+I2(g)的化学平衡常 数为
| A.0.02 | B.50 | C.100 | D.无法确定 |
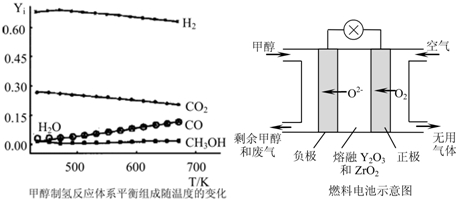
 H2+I2
H2+I2