题目内容
(16分) 373 K时,某1 L密闭容器中加入1molPCl5发生如下可逆反应:
 PCl5 (g)
PCl3(g) + Cl2 (g)。其中物质PCl3的物质的量变化如图所示。
PCl5 (g)
PCl3(g) + Cl2 (g)。其中物质PCl3的物质的量变化如图所示。
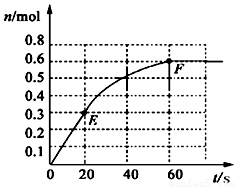
(1)前20 s内PCl5(g)的平均反应速率为
(2)373 K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入1mol的PCl5,与原平衡比较,新平衡时PCl5的转化率 (填“增大”或“减小”,下同)。PCl5的平衡浓度
(4)将原平衡升温至473 K,重新达平衡时(其他条件不变),PCl3的平衡浓度为PCl5的3倍,该反应的正反应为 (填“放热反应”或 “吸热反应”),为增大平衡体系中Cl2的物质的量,下列措施正确的是(其它条件相同)
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入PCl3
【答案】
(16分)
(1) 0.005mol·L-1·s-1 (3分) (2) 0.9 mol·L-1 (3分)
(3) 减小 增大 (各2分)
(4)吸热 (2分) a b(各2分,如果有选错都为0分)
【解析】

练习册系列答案
相关题目