题目内容
综合处理“工业三废”,有利于保护环境,节约资源。
(1)为处理某工厂的工业废气(主要含N2、SO2、NO、CO,不考虑其他成分),设计了如下流程:已知:
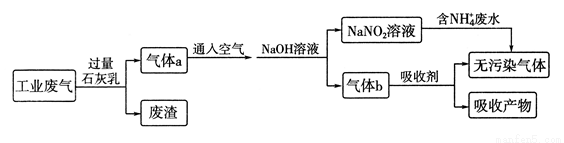
NO+NO2+2NaOH=2NaNO2+H2O;
2NO2+2NaOH=NaNO3+NaNO2+H2O。
①废渣的成分为_____________(填化学式)。
② 通入空气不能过量,原因是______________________。
通入空气不能过量,原因是______________________。
③吸收剂所吸收的气体主要是______________。
④处理含NH4+废水时,发生反应的离子方程式为_____________________。
(2)某无色工业废水中可能含有NH4+、Na+、Al3+、Cu2+、Cl-、SO42-、CO32-等离子中的几种离子。为确定其成分,设计如下实验:
a.取10 mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到0.04 mol白色沉淀,向滤液中加入AgNO3溶液无沉淀产生。
b.另取10mL该废水于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体,最后沉淀完全溶解。沉淀和气体的物质的量随加入NaOH溶液体积的变化关系如下图所示。(不考虑沉淀、气体的溶解和损失)

根据上述实验和图表数据:
①该废水中一定含有的离子有_______________(填离子符号)。
②实验室配制100mL所需浓度的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要________________(填仪器名称)。
③图中a=_________。
 全能测控期末小状元系列答案
全能测控期末小状元系列答案已知H2(g)+Br2(g)=2HBr(g) △H=-102 kJ·mol-1,其它相关数据如下表:
H2(g) | Br2(g) | HBr(g) | ||
1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 | |
则表中a为
A.230 B.200 C.404 D.260





