题目内容
以煤为原料,经化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ?mo1-1
①该反应在高温下______自发进行(填“能”或“不能”)
②恒温下,在容积不变的密闭容器中,进行如上可逆反应.一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的是:______.
Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量,ⅣCO物质的量浓度
A.只有Ⅳ.
B只有Ⅰ和Ⅳ
C.只有Ⅱ和Ⅲ
D.只有Ⅰ、Ⅱ、Ⅲ和Ⅳ
(2)水煤气再进一步反应可制取氢气.反应为H2O(g)+CO(g)?H2(g)+CO2(g),某温度下该反应的平衡常数K=4/9.该温度下在甲、乙、丙三个恒温密闭容器中,只投入H2(g)和CO2(g),其起始浓度下表所示.下列判断不正确的是______
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mo1/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/moI/L | 0.010 | 0.010 | 0.020 |
B.平衡时甲中和丙中的H2的转化率均是60%
C.平衡时,丙中的c(CO2)是甲中的2倍,是0.102mol/L
D.平衡时,乙中的CO2的转化率大于60%
(3)目前工业上有一种方法是用CO2来制取甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应进行过程中能量的变化.在体积为1L的恒容密闭容器中,冲入1mo1CO2和3mo1H2反
①下列措施中能使平衡混合物中c(CH3OH))增大的是______
A.升高温度
B.冲入He(g)使体系压强增大
C.将H2O(g)从体系中分离出来
D.再冲入1mo1CO2和3mo1H2
②在温度T1时,当反应达到平衡时,测得n(H2)=2.4mo1;其他条件不变,在温度T2时,当反应达到平衡时,测得n(CO2)=0.82mol,则得T1______T2(填“>”、“<”或“=”)
(4)在一定条件下科学家从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇(常温下为液体).CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mo1、△H=-285.5kJmo1
①写出工业上以CO2、H2合成CH3OH和液态水的热化学方程式:______
②该转化的积极意义是______
有人提出,可以设计反应CO2=C+O2(△H>0、△S<0)来消除CO2对环境的影响.请你判断是否可行并说出理由:______.

【答案】分析:(1)①该反应为熵增大,焓增大的反应,由△G=△H-T△S判断;
②根据达到平衡时的特征“等”、“定”结合反应方程式的特征判断是否达到平衡状态;
(2)反应H2O(g)+CO(g)?H(g)+CO2(g)中,反应物和生成物的体积相等,压强对平衡移动无影响,从等效平衡的角度结合浓度对平衡的影响分析;
(3)①使平衡混合物中c(CH3OH))增大,应使平衡向正反应方向移动;
②反应为放热反应,升高温度平衡向逆反应方向移动;
(4)①利用盖斯定律计算反应热,并书写热化学方程式;
②根据△G=△H-T△S判断反应能否自发进行.
解答:解:(1)该反应为熵增大,焓增大的反应,由△G=△H-T△S,△G<0反应可自发进行,可知该反应在高温时可以自发进行,常温下难以自发进行,故答案为:①能;
②Ⅰ由于有固体参加反应,当混合气体的密度不变时,气体的质量不变,说明达到平衡状态;
Ⅱ反应前后气体的体积不等,当容器内气体的压强不变时说明达到平衡状态;
Ⅲ反应前后气体的体积不等,混合气体的总物质的量不变,说明达到平衡状态;
ⅣCO物质的量浓度不变,说明达到平衡状态,则Ⅰ、Ⅱ、Ⅲ和Ⅳ都可说明达到平衡状态,
故答案为:D;
(2)A.丙中浓度最大,甲中浓度最小,浓度越大,反应速率越大,则反应开始时,丙中的反应速率最快,甲中的反应最慢,故A正确;
B. 以甲计算:
H2O(g)+CO(g)?H2(g)+CO2(g)
起始:0 0 0.010 0.010
转化:x x x x
平衡:x x 0.01-x 0.01-x
则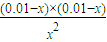 =
= ,
,
x=0.006,则平衡时甲中的H2的转化率均是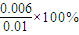 =60%,由于甲和丙的气体的比值相同,为等效平衡状态,则丙中H2的转化率也为60%,故B正确;
=60%,由于甲和丙的气体的比值相同,为等效平衡状态,则丙中H2的转化率也为60%,故B正确;
C.由B计算可知,平衡时,丙中的c(CO2)是甲中的2倍,应为2×(0.01-0.006)mol/L=0.008mol/L,故C错误;
D.乙与甲相比较,相当于在甲的基础上通入H2,则平衡向逆反应方向移动,平衡时,乙中的CO2的转化率大于60%,故D正确.
故答案为:C;
(3)①反应物总能量大于生成物总能量,该反应的正反应放热,则
A.升高温度,平衡向逆反应方向移动,平衡混合物中c(CH3OH)减小,故A错误;
B.冲入He(g)使体系压强增大,但反应物的浓度不变,平衡不移动,故B错误;
C.将H2O(g)从体系中分离出来,生成物浓度减小,则平衡向正反应方向移动,平衡混合物中c(CH3OH))增大,故C正确;
D.再冲入1mo1CO2和3mo1H2,相当于在原来基础上增大压强,平衡向正反应方向移动,平衡混合物中c(CH3OH))增大,故D正确.
故答案为:CD;
②在温度T1时,当反应达到平衡时,测得n(H2)=2.4mo1,则平衡时n(CO2)=1mol- ×(3mol-2.4mol)=0.8mol;其他条件不变,在温度T2时,当反应达到平衡时,测得n(CO2)=0.82mol,说明平衡向正反应方向移动,反应为放热反应,降低温度平衡向正反应方向移动,故答案为:>;
×(3mol-2.4mol)=0.8mol;其他条件不变,在温度T2时,当反应达到平衡时,测得n(CO2)=0.82mol,说明平衡向正反应方向移动,反应为放热反应,降低温度平衡向正反应方向移动,故答案为:>;
(4)①甲醇和氢气的燃烧热书写其热化学方程式分别为:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l),△H1=-1451kJ/mol;
②2H2(g)+O2(g)=2H2O(l),△H2=-571.6KJ/mol,
根据盖斯定律,反应CO2(g)+3H2(g)═CH3OH(l)+H2O(l)
可以看成是方程式 ×②-①×
×②-①× ,所以△H=
,所以△H= ×(-571.6KJ/mol)-(-1451kJ/mol)×
×(-571.6KJ/mol)-(-1451kJ/mol)× =-131.9KJ/mol,
=-131.9KJ/mol,
故答案为:CO2(g)+3H2(g)═CH3OH(l)+H2O(l),△H=-131.9KJ/mol;
②该反应消耗二氧化碳,可降低温室效应,生成甲醇,可弥补资源短缺,故答案为:可降低温室效应和弥补资源短缺;
③该反应是一个焓增、熵减的反应,则△G=△H-T△S>0,不能自发进行,
故答案为:不可行,该反应是一个焓增、熵减的反应,所以不能自发进行.
点评:本题考查化学平衡以及反应热的计算,题目难度较大,本题注意利用三段式法计算,易错点为(2),注意对等效平衡的理解和运用.
②根据达到平衡时的特征“等”、“定”结合反应方程式的特征判断是否达到平衡状态;
(2)反应H2O(g)+CO(g)?H(g)+CO2(g)中,反应物和生成物的体积相等,压强对平衡移动无影响,从等效平衡的角度结合浓度对平衡的影响分析;
(3)①使平衡混合物中c(CH3OH))增大,应使平衡向正反应方向移动;
②反应为放热反应,升高温度平衡向逆反应方向移动;
(4)①利用盖斯定律计算反应热,并书写热化学方程式;
②根据△G=△H-T△S判断反应能否自发进行.
解答:解:(1)该反应为熵增大,焓增大的反应,由△G=△H-T△S,△G<0反应可自发进行,可知该反应在高温时可以自发进行,常温下难以自发进行,故答案为:①能;
②Ⅰ由于有固体参加反应,当混合气体的密度不变时,气体的质量不变,说明达到平衡状态;
Ⅱ反应前后气体的体积不等,当容器内气体的压强不变时说明达到平衡状态;
Ⅲ反应前后气体的体积不等,混合气体的总物质的量不变,说明达到平衡状态;
ⅣCO物质的量浓度不变,说明达到平衡状态,则Ⅰ、Ⅱ、Ⅲ和Ⅳ都可说明达到平衡状态,
故答案为:D;
(2)A.丙中浓度最大,甲中浓度最小,浓度越大,反应速率越大,则反应开始时,丙中的反应速率最快,甲中的反应最慢,故A正确;
B. 以甲计算:
H2O(g)+CO(g)?H2(g)+CO2(g)
起始:0 0 0.010 0.010
转化:x x x x
平衡:x x 0.01-x 0.01-x
则
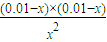 =
= ,
,x=0.006,则平衡时甲中的H2的转化率均是
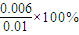 =60%,由于甲和丙的气体的比值相同,为等效平衡状态,则丙中H2的转化率也为60%,故B正确;
=60%,由于甲和丙的气体的比值相同,为等效平衡状态,则丙中H2的转化率也为60%,故B正确;C.由B计算可知,平衡时,丙中的c(CO2)是甲中的2倍,应为2×(0.01-0.006)mol/L=0.008mol/L,故C错误;
D.乙与甲相比较,相当于在甲的基础上通入H2,则平衡向逆反应方向移动,平衡时,乙中的CO2的转化率大于60%,故D正确.
故答案为:C;
(3)①反应物总能量大于生成物总能量,该反应的正反应放热,则
A.升高温度,平衡向逆反应方向移动,平衡混合物中c(CH3OH)减小,故A错误;
B.冲入He(g)使体系压强增大,但反应物的浓度不变,平衡不移动,故B错误;
C.将H2O(g)从体系中分离出来,生成物浓度减小,则平衡向正反应方向移动,平衡混合物中c(CH3OH))增大,故C正确;
D.再冲入1mo1CO2和3mo1H2,相当于在原来基础上增大压强,平衡向正反应方向移动,平衡混合物中c(CH3OH))增大,故D正确.
故答案为:CD;
②在温度T1时,当反应达到平衡时,测得n(H2)=2.4mo1,则平衡时n(CO2)=1mol-
 ×(3mol-2.4mol)=0.8mol;其他条件不变,在温度T2时,当反应达到平衡时,测得n(CO2)=0.82mol,说明平衡向正反应方向移动,反应为放热反应,降低温度平衡向正反应方向移动,故答案为:>;
×(3mol-2.4mol)=0.8mol;其他条件不变,在温度T2时,当反应达到平衡时,测得n(CO2)=0.82mol,说明平衡向正反应方向移动,反应为放热反应,降低温度平衡向正反应方向移动,故答案为:>;(4)①甲醇和氢气的燃烧热书写其热化学方程式分别为:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l),△H1=-1451kJ/mol;
②2H2(g)+O2(g)=2H2O(l),△H2=-571.6KJ/mol,
根据盖斯定律,反应CO2(g)+3H2(g)═CH3OH(l)+H2O(l)
可以看成是方程式
 ×②-①×
×②-①× ,所以△H=
,所以△H= ×(-571.6KJ/mol)-(-1451kJ/mol)×
×(-571.6KJ/mol)-(-1451kJ/mol)× =-131.9KJ/mol,
=-131.9KJ/mol,故答案为:CO2(g)+3H2(g)═CH3OH(l)+H2O(l),△H=-131.9KJ/mol;
②该反应消耗二氧化碳,可降低温室效应,生成甲醇,可弥补资源短缺,故答案为:可降低温室效应和弥补资源短缺;
③该反应是一个焓增、熵减的反应,则△G=△H-T△S>0,不能自发进行,
故答案为:不可行,该反应是一个焓增、熵减的反应,所以不能自发进行.
点评:本题考查化学平衡以及反应热的计算,题目难度较大,本题注意利用三段式法计算,易错点为(2),注意对等效平衡的理解和运用.

练习册系列答案
相关题目
 (1)食品和药品关系人的生存和健康.
(1)食品和药品关系人的生存和健康.