题目内容
(1)0.02 mol·L-1的HCN溶液与0.02 mol·L-1 NaCN溶液等体积混合,已知该混合溶液中c (Na+)> c(CN-),用“>、<、=”符号填空
①溶液中c(OH -) c(H +) ② c(HCN) c(CN-)
(2)常温下,向明矾溶液中滴入Ba(OH)2溶液至SO42- 刚好完全沉淀时,溶液
pH 7,(用“>、<、=”符号填空)反应的离子方程式为__________________________________。
(3)BaCO3分别加入:① 30mL水 ②10mL 0.2mol/LNa2CO3溶液 ③50mL 0.01mol/L
氯化钡溶液 ④100mL 0.01mol/L盐酸中溶解至溶液饱和。请确定各溶液中
Ba2+的浓度由大到小的顺序为:___________________________________________。
(1)① > (2分), ② > (2分);
(2)> (2分), Al3++2SO42-+2Ba2++4OH- = 2BaSO4↓+ AlO2- (2分);
(3) ③④①② (2分)
【解析】(1)根据电荷守恒可知c(Na+)+c(H+)=c(OH-)+c(CN-),所以当c (Na+)> c(CN-)时,c(OH -)>c(H +),这说明溶液显碱性,所以HCN的电离程度小于NaCN的水解程度,因此c(HCN) >c(CN-)。
(2)明矾是KAl(SO4)2,当SO42- 刚好完全沉淀时,需要2molBa(OH)2溶液,则此时铝离子恰好生成KAlO2,KAlO2水解显碱性,反应式为Al3++2SO42-+2Ba2++4OH- = 2BaSO4↓+ AlO2-。
(3)BaCO3(s) Ba2+(aq)+CO32-(aq)碳酸钡的在溶液中存在溶解平衡,根据溶度积常数可知CO32-浓度越大,钡离子浓度就越小、平衡向右,可以增大钡离子的浓度,所以正确的顺序是③④①②
Ba2+(aq)+CO32-(aq)碳酸钡的在溶液中存在溶解平衡,根据溶度积常数可知CO32-浓度越大,钡离子浓度就越小、平衡向右,可以增大钡离子的浓度,所以正确的顺序是③④①②

在催化剂作用下,乙酸可通过两步反应得乙烷,反应原理如下:
① CH3COOH+2H2→CH3CH2OH+H2O ② CH3CH2OH+H2→CH3CH3+H2O
③ CH3COOH+3H2→CH3CH3+2H2O 在反应过程中乙酸和乙醇会生成乙酸乙酯。为研究分别考查了加Mo(钼)和不加Mo负载型Ni(镍)催化剂催化效能,某文献记载的数据如下:
| 乙酸转化率 | 未反应的含氧化合物含量 | |||||
| 乙酸 | 乙醇 | |||||
| 温度 / ℃ | Mo16Ni6 | Ni6 | Mo16Ni6 | Ni6 | Mo16Ni6 | Ni6 |
| 240 | 87.2 | 21.8 | 0.53 | 3.24 | 1.03 | 0.14 |
| 260 | 89.1 | 27.2 | 0.45 | 3.02 | 0.99 | 0.19 |
下列叙述不正确的是
A.上述①②③三反应均属于加成反应 B.上述①②③三反应均属于还原反应
C.乙酸加氢脱氧反应260℃比240℃进行更有利 D.Mo16Ni6催化性能比Ni6好
(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.用于合成氨的工业煤气中含有H2S、C2H5SH(乙酸醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理。
H2S+ZnO=ZnS+H2O;C2H5SH+ZnO=ZnS+C2H4+H2O
C2H5SH+H2=C2H6+H2S;COS+H2=CO+H2S;CS2+4H2=CH4+2H2S
(1)钴原子在基态时核外电子排布式为 。
(2)下列有关分子结构的说法正确的是 。
A.C2H4分子中有5个![]() 键处1个
键处1个![]() 键
键
B.COS分子(结构如右图)中键能C=O>C=S
C.H2S分子呈V形结构
D.CH4、C2H6分子中碳原子均采用sp3杂化
(3)下列有关说法不正确的是 。
A.H2O、CO、COS均是极性分子
B.相同压强下沸点:Cs2>COS>CO2
C.相同压强下沸点:C2H5SH>C2H5OH
D.相同压强下沸点:CO>N2
(4)![]() -ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
-ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于 。
(6)钼的一种配合物化学式为:Na3[Mo(CN)8]·8H2O,中心原子的配位数为 。
B.烃醛结合反应有机合成中颇为重要,绿色催化剂的固体铌酸酸倍受研究者关注。铌酸具有较高的催化活性及稳定性。反应原理如下:
实验方法是在25mL烧瓶中加入铌酸、10mL甲醇和 0.5mL苯甲醛,在回流状态下反应2h,反应的产率和转化率均非常高。
(1)采用回流反应2h的目的是 。
(2)在反应中甲醇需过量,其原因是 。
(3)不同铌酸用量对产率和转化率影响,如下表:
| 铌酸用量/mol | 0.01 | 0.02 | 0.03 | 0.05 | 0.1 | 0.15 | 0.2 | 0.6 |
| 产率% | 87.3 | 88.2 | 90.3 | 94.2 | 92.9 | 93.1 | 91.8 | 92.3 |
| 转化率% | 89.7 | 92.1 | 93.9 | 98.9 | 94.9 | 95.7 | 93.9 | 94.3 |
在上述苯甲醛与甲醇缩合反应实验中催化剂铌酸的最佳用量为 。
(4)催化剂的回收利用性能是考察催化剂的一项极为重要的指标。铌酸催化剂循环使用次数对产率的影响如右下图,这说明铌酸催化剂的优点之一是 。
(5)用铌酸作催化剂时,不同的醛与甲醇的缩合反应的转化率和产率如下表:
| 序号 | 醛 | 醇 | 转化率% | 产率% |
| 1 | 邻羟基苯甲醛 | 甲醇 | 94.3 | 89.6 |
| 2 | 邻羟基苯甲醛 | 甲醇 | 93.6 | 88.7 |
| 3 | 邻氯苯甲醛 | 甲醇 | 93.1 | 87.3 |
| 4 | 间硝基苯甲醛 | 甲醇 | 54.2 | 34.1 |
| 5 | 邻硝基苯甲醛 | 甲醇 | 89.9 | 79.5 |
| 6 | 对硝基苯甲醛 | 甲醇 | 65.7 | 41.9 |
从表中得出的不同的醛与甲醇缩合反应影响转化率和产率的规律是 。
在催化剂作用下乙酸可通过两步反应得乙烷,反应原理如下:
①CH3COOH+2H2→CH3CH2OH+H2O
②CH3CH2OH+H2→CH3CH3+H2O
③CH3COOH+3H2→CH3CH3+2H2O
在反应过程中乙酸和乙醇会生成乙酸乙酯。为研究分别考查了加Mo(钼)和不加Mo负载型Ni(镍)催化剂催化效能,某文献记载的数据如下:
|
|
乙酸转化率 |
未反应的含氧化合物含量 |
||||
|
乙酸 |
乙醇 |
|||||
|
温度/℃ |
Mo16Ni6 |
Ni6 |
Mo16Ni6 |
Ni6 |
Mo16Ni6 |
Ni6 |
|
240 |
87.2 |
21.8 |
0.53 |
3.24 |
1.03 |
0.14 |
|
260 |
89.1 |
27.2 |
0.45 |
3.02 |
0.99 |
0.19 |
下列说法不正确的是 ( )
A.上述①②③三反应均属于加成反应
B.上述①②③三反应均属于还原反应
C.乙酸加氢脱氧反应260℃比240℃下进行更有利
D.Mo16Ni6催化性能比Ni6好
(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.用于合成氨的工业煤气中含有H2S、C2H5SH(乙酸醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理。
H2S+ZnO=ZnS+H2O;C2H5SH+ZnO=ZnS+C2H4+H2O
C2H5SH+H2=C2H6+H2S;COS+H2=CO+H2S;CS2+4H2=CH4+2H2S
(1)钴原子在基态时核外电子排布式为 。
(2)下列有关分子结构的说法正确的是 。
A.C2H4分子中有5个 键处1个
键处1个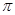 键
键
B.COS分子(结构如右图)中键能C=O>C=S
C.H2S分子呈V形结构
D.CH4、C2H6分子中碳原子均采用sp3杂化
(3)下列有关说法不正确的是 。
A.H2O、CO、COS均是极性分子
B.相同压强下沸点:Cs2>COS>CO2
C.相同压强下沸点:C2H5SH>C2H5OH
D.相同压强下沸点:CO>N2
(4)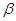 -ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
-ZnS的晶胞结构如右图,晶胞中S2-数目为: 个。
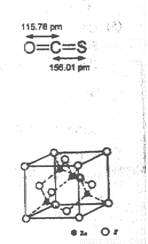
(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于 。
(6)钼的一种配合物化学式为:Na3[Mo(CN)8]·8H2O,中心原子的配位数为 。
B.烃醛结合反应有机合成中颇为重要,绿色催化剂的固体铌酸酸倍受研究者关注。铌酸具有较高的催化活性及稳定性。反应原理如下:
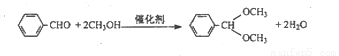
实验方法是在25mL烧瓶中加入铌酸、10mL甲醇和 0.5mL苯甲醛,在回流状态下反应2h,反应的产率和转化率均非常高。
(1)采用回流反应2h的目的是 。
(2)在反应中甲醇需过量,其原因是 。
(3)不同铌酸用量对产率和转化率影响,如下表:
|
铌酸用量/mol |
0.01 |
0.02 |
0.03 |
0.05 |
0.1 |
0.15 |
0.2 |
0.6 |
|
产率% |
87.3 |
88.2 |
90.3 |
94.2 |
92.9 |
93.1 |
91.8 |
92.3 |
|
转化率% |
89.7 |
92.1 |
93.9 |
98.9[来源:Zxxk.Com] |
94.9 |
95.7 |
93.9 |
94.3 |
在上述苯甲醛与甲醇缩合反应实验中催化剂铌酸的最佳用量为 。
(4)催化剂的回收利用性能是考察催化剂的一项极为重要的指标。铌酸催化剂循环使用次数对产率的影响如右下图,这说明铌酸催化剂的优点之一是 。
(5)用铌酸作催化剂时,不同的醛与甲醇的缩合反应的转化率和产率如下表:
|
序号 |
醛 |
醇 |
转化率% |
产率% |
|
1 |
邻羟基苯甲醛 |
甲醇 |
94.3 |
89.6 |
|
2 |
邻羟基苯甲醛 |
甲醇 |
93.6 |
88.7 |
|
3 |
邻氯苯甲醛 |
甲醇 |
93.1 |
87.3 |
|
4 |
间硝基苯甲醛 |
甲醇 |
54.2 |
34.1 |
|
5 |
邻硝基苯甲醛 |
甲醇 |
89.9 |
79.5 |
|
6 |
对硝基苯甲醛 |
甲醇 |
65.7 |
41.9 |

从表中得出的不同的醛与甲醇缩合反应影响转化率和产率的规律是 。