题目内容
某温度下,C和水在密闭容器中发生下列反应:C(s)+H2O(g)?CO(g)+H2(g),CO(g)+H2O(g)?CO2(g)+H2(g)当反应达平衡时,测得c(H2)=1.9mol/L,c(CO)=0.1mol/L,则CO2的浓度为( )A.0.1 mol/L
B.0.9 mol/L
C.1.8 mol/L
D.1.9 mol/L
【答案】分析:氢气来源C与水的反应,CO与水的反应,二氧化碳来源与CO与水的反应,平衡时CO为C与水反应生成CO减去CO与水反应消耗的CO,令碳与水反应生成的氢气的浓度为amol/L,则生成的CO为amol/L,令CO与水反应生成氢气的浓度为bmol/L,则生成的二氧化碳的浓度为bmol/L,消耗的CO浓度为bmol/L,结合氢气、CO浓度计算.
解答:解:令碳与水反应生成的氢气的浓度为amol/L,则生成的CO为amol/L,令CO与水反应生成氢气的浓度为bmol/L,则生成的二氧化碳的浓度为bmol/L,消耗的CO浓度为bmol/L,
平衡时氢气的浓度为1.9mol/L,则amol/L+bmol/L=1.9mol/L,
平衡时CO的浓度为0.1mol/L,则amol/L-bmol/L=0.1mol/L,
联立解得a=1,b=0.9,故CO2的浓度为0.9mol/L,
故选B.
点评:本题考查化学平衡的有关计算,难度中等,清楚反应过程是关键.
解答:解:令碳与水反应生成的氢气的浓度为amol/L,则生成的CO为amol/L,令CO与水反应生成氢气的浓度为bmol/L,则生成的二氧化碳的浓度为bmol/L,消耗的CO浓度为bmol/L,
平衡时氢气的浓度为1.9mol/L,则amol/L+bmol/L=1.9mol/L,
平衡时CO的浓度为0.1mol/L,则amol/L-bmol/L=0.1mol/L,
联立解得a=1,b=0.9,故CO2的浓度为0.9mol/L,
故选B.
点评:本题考查化学平衡的有关计算,难度中等,清楚反应过程是关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
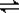 ?CO(g)+H2(g), CO(g)+H2O(g)?
?CO(g)+H2(g), CO(g)+H2O(g)?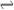 CO(g)+H2,CO(g)+H2O(g)
CO(g)+H2,CO(g)+H2O(g)
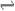 CO2(g)+H2(g)当反应达平衡时,测得c(H2)=1.9mol/L,c(CO2)=0.9mol/L,则CO的浓度为( )
CO2(g)+H2(g)当反应达平衡时,测得c(H2)=1.9mol/L,c(CO2)=0.9mol/L,则CO的浓度为( )