题目内容
 如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )
如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )| A、该图体现出原子核外电子层呈现周期性变化 |
| B、原子半径:W>R>X |
| C、W的氢化物与R的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W |
| D、R、Z形成的化合物中可能含有共价键 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答:
解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,
A.该图体现出原子核外最外层电子数的周期性变化,而不是电子层,故A错误;
B.同周期自左而右,原子半径减小,电子层越多原子半径越大,故原子半径S>Cl>O,故B错误;
C.W的氢化物与R的氢化物水溶液的酸性相比较,HCl酸性较强,Cl的非金属性较强,故C错误;
D.R、Z形成的化合物可为Na2Sx,存在S-S键,为共价键,故D正确.
故选D.
A.该图体现出原子核外最外层电子数的周期性变化,而不是电子层,故A错误;
B.同周期自左而右,原子半径减小,电子层越多原子半径越大,故原子半径S>Cl>O,故B错误;
C.W的氢化物与R的氢化物水溶液的酸性相比较,HCl酸性较强,Cl的非金属性较强,故C错误;
D.R、Z形成的化合物可为Na2Sx,存在S-S键,为共价键,故D正确.
故选D.
点评:本题考查原子结构与元素周期律知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构,难度中等.

练习册系列答案
相关题目
下列所用除杂的试剂和操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 所用试剂 | 操作方法 |
| ① | 乙烯 | 二氧化硫 | 氯水 | 洗气 |
| ② | 乙炔 | 硫化氢 | 氢氧化钠溶液 | 洗气 |
| ③ | 苯 | 苯酚 | 溴水 | 过滤 |
| ④ | 溴苯 | 液溴 | 氢氧化钠溶液 | 分液 |
| A、②④ | B、①④ | C、②③ | D、①③ |
在无色透明的溶液中能大量共存的是( )
| A、HCO3-、Na+、OH-、Cl- |
| B、Ca2+、NO3-、SO42-、CO32- |
| C、Fe2+、Na+、H+、NO3- |
| D、Cl-、Mg2+、Na+、SO42- |
把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A(g)+B(g)?2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L?min),下列说法错误的是( )
| A、x=2 |
| B、B的转化率为20% |
| C、平衡时A的浓度为0.8mol/L |
| D、恒温达平衡时容器内的压强与开始时相等 |
下列实验设计及其对应的离子方程式均正确的是( )
| A、NaHSO4与NaOH溶液反应:H++OH-=H2O |
| B、少量的Fe与稀硝酸反应:Fe+2H+=Fe2++H2↑ |
| C、实验室利用氢氧化钙固体和氯化铵反应制备氨气:NH4++OH-=NH3↑+H2O |
| D、金属Na与水反应:Na+H2O=Na++OH-+H2↑ |
下列有关银镜反应实验的说法正确的是( )
| A、试管要用浓硫酸和蒸馏水洗涤 |
| B、采用水浴加热,不能直接加热 |
| C、向2%的稀氨水中滴入2%的硝酸银溶液,配得银氨溶液 |
| D、可用浓盐酸洗去银镜 |
苯分子中不存在碳碳单、双键的交替结构,下列可以作为证据的事实是( )
①苯不能使酸性KMnO4溶液褪色
②苯不能因发生化学反应而使溴的四氯化碳溶液褪色
③苯在加热和有催化剂存在的条件下能与H2加成生成环已烷
④苯分子中碳碳键长完全相等
⑤邻二氯苯( )只有一种
)只有一种
⑥间二氯苯(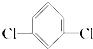 )只有一种.
)只有一种.
①苯不能使酸性KMnO4溶液褪色
②苯不能因发生化学反应而使溴的四氯化碳溶液褪色
③苯在加热和有催化剂存在的条件下能与H2加成生成环已烷
④苯分子中碳碳键长完全相等
⑤邻二氯苯(
 )只有一种
)只有一种⑥间二氯苯(
 )只有一种.
)只有一种.| A、①② | B、①⑤ |
| C、③④⑤⑥ | D、①②④⑤ |
下列有关化学用语使用正确的是( )
A、甲烷分子的球棍模型: |
B、H2O2的电子式: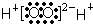 |
C、硫原子的结构示意图: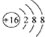 |
| D、次氯酸分子的结构式:H-O-Cl |
下列事实不能用勒夏特列原理解释的是( )
| A、打开啤酒瓶盖,瓶口冒出大量气泡 |
| B、合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率 |
| C、由H2、I2(g)、HI(g)气体组成的平衡体系减压后颜色变浅 |
| D、工业制取金属钾Na(l)+KCl(l)?NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |