题目内容
下列实验中,溶液颜色有明显变化的是( )
| A.少量明矾溶液加入到过量NaOH溶液中 |
| B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C.少量Na2O2固体加入到过量NaHSO4溶液中 |
| D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液 |
B
解析

练习册系列答案
相关题目
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是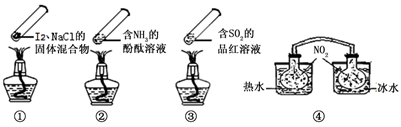
| A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差 |
| B.加热时,②、③中的溶液均变红,冷却后又都变为无色 |
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅(已知:2NO2(g)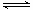 N2O4(g)△H<0) N2O4(g)△H<0) |
| D.四个“封管实验”中都有可逆反应发生 |
下列因果关系叙述正确的是( )
| A.纯碱是一种碱,故可用于去油污 |
| B.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| C.Na的金属性比Mg强,故可用Na与MgCl2溶液反应制取Mg |
| D.SiO2能与氢氟酸及碱反应,故SiO2是两性氧化物 |
下列叙述正确的是
| A.Na2O和Na2O2组成元素相同,化学性质也相同 |
| B.相同质量的铁粉分别与足量稀硫酸和稀硝酸反应,消耗酸的物质的量相同 |
| C.Si、P、S、Cl的得电子能力及其最高价氧化物对应水化物的酸性均依次增强 |
| D.在常温下,浓硫酸、浓硝酸与铁均不发生反应,故能用铁罐储运 |
下列说法错误的是
| A.碳、硫单质在加热条件下都能与浓硝酸、浓硫酸发生反应 |
| B.氮氧化物、二氧化硫是形成酸雨的主要物质 |
| C.二氧化硫具有还原性,因此不能用浓硫酸干燥 |
| D.硅在自然界中主要以氧化物和硅酸盐的形式存在 |
下列叙述和解释正确的是
| 选项 | 叙述 | 原因或解释 |
| A | SO2通入氢氧化钠酚酞溶液中,溶液褪色 | SO2具有漂白作用 |
| B | 将浓硫酸滴到蔗糖表面,固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| C | 过滤时应用玻璃棒引流和搅拌 | 防止滤液溅出和缩短过滤时间 |
| D | 浓硝酸应保存在棕色瓶中 | 浓硝酸易挥发 |
下列由相关实验现象所推出的结论正确的是( )
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42— |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
如图所示是一套实验室制气装置,用于发生、干燥和收集气体。下列各组物质中能利用这套装置进行实验的是( )
| A.铜屑和稀硝酸 | B.二氧化锰和浓盐酸 |
| C.用浓氨水和生石灰反应 | D.碳酸钙和稀盐酸 |
下列叙述中正确的是( )
| A.液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |