题目内容
(13分)
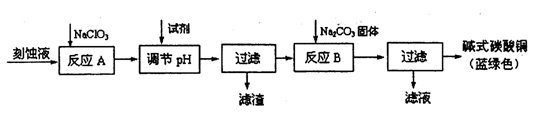
用菱锌矿(主要成分为碳酸锌,还含有Fe2+、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的一种流程如下。

(1) 在反应3前要将菱锌矿研磨,其目的是。
(2) 反应4将Fe2+ 氧化为Fe3+,该反应的离子方程式为。
(3) 加入氧化锌调节至pH=4.5,反应5的离子方程式为。
(4) 锌粉不在反应4之前加入的原因是。
(5) 若用石墨做电极电解滤液Y,则可以得到参与本流程反应的物质有。
用菱锌矿(主要成分为碳酸锌,还含有Fe2+、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的一种流程如下。

(1) 在反应3前要将菱锌矿研磨,其目的是。
(2) 反应4将Fe2+ 氧化为Fe3+,该反应的离子方程式为。
(3) 加入氧化锌调节至pH=4.5,反应5的离子方程式为。
(4) 锌粉不在反应4之前加入的原因是。
(5) 若用石墨做电极电解滤液Y,则可以得到参与本流程反应的物质有。

(1)将菱锌矿研磨,是为了增大物质的表面积,使接触面积增大从而使反应速率增大。(2)反应1的溶液中含有次氯酸钠,反应3的溶液中含有盐酸和二价铁,酸性溶液中次氯酸钠具有强氧化性与亚铁离子反应,反应的离子方程式为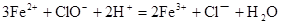 。(3)反应4的溶液中含有三价铁离子,氢离子,所以加入氧化锌,氧化锌与氢离子反应的离子反应方程式为
。(3)反应4的溶液中含有三价铁离子,氢离子,所以加入氧化锌,氧化锌与氢离子反应的离子反应方程式为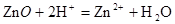 ,红褐色沉淀来自于三价铁离子的水解离子反应方程式为
,红褐色沉淀来自于三价铁离子的水解离子反应方程式为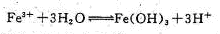 。(4)若锌粉在反应4之前加入则锌粉会与氢离子和三价铁反应增加锌粉的用量(5)滤液Y的主要成分是氯化钠、氯化锌,电解的时候会产生氢气、氯气和锌单质。
。(4)若锌粉在反应4之前加入则锌粉会与氢离子和三价铁反应增加锌粉的用量(5)滤液Y的主要成分是氯化钠、氯化锌,电解的时候会产生氢气、氯气和锌单质。
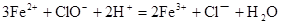 。(3)反应4的溶液中含有三价铁离子,氢离子,所以加入氧化锌,氧化锌与氢离子反应的离子反应方程式为
。(3)反应4的溶液中含有三价铁离子,氢离子,所以加入氧化锌,氧化锌与氢离子反应的离子反应方程式为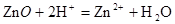 ,红褐色沉淀来自于三价铁离子的水解离子反应方程式为
,红褐色沉淀来自于三价铁离子的水解离子反应方程式为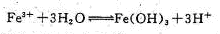 。(4)若锌粉在反应4之前加入则锌粉会与氢离子和三价铁反应增加锌粉的用量(5)滤液Y的主要成分是氯化钠、氯化锌,电解的时候会产生氢气、氯气和锌单质。
。(4)若锌粉在反应4之前加入则锌粉会与氢离子和三价铁反应增加锌粉的用量(5)滤液Y的主要成分是氯化钠、氯化锌,电解的时候会产生氢气、氯气和锌单质。
练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目