��Ŀ����
��12�֣�830Kʱ�����ܱ������з������п��淴Ӧ��CO��g��+H2O��g�� CO2��g��+H2��g�� ��H��0�����Իش��������⣺
CO2��g��+H2��g�� ��H��0�����Իش��������⣺
��1������ʼʱc��CO��="2" mol��L-1��c��H2O��="3" mol��L-1���ﵽƽ��ʱCO��ת����Ϊ60%�����ڸ��¶��£��÷�Ӧ��ƽ�ⳣ��K= ���� .
��2������ͬ�¶��£�����ʼʱc��CO��="1" mol��L-1��c��H2O��="2" mol��L-1����Ӧ����һ��ʱ����H2��Ũ��Ϊ0.5 mol��L-1�����ʱ�÷�Ӧ�Ƿ�ﵽƽ��״̬ ����ǡ��롰������ʱv������ v���棩������ڡ���С�ڡ����ڡ��������жϵ�������
��������
��3���������¶ȣ��÷�Ӧ��Kֵ�� ���÷�Ӧ�Ļ�ѧ��Ӧ���ʽ� �� �����������С�����䡱����
 CO2��g��+H2��g�� ��H��0�����Իش��������⣺
CO2��g��+H2��g�� ��H��0�����Իش��������⣺��1������ʼʱc��CO��="2" mol��L-1��c��H2O��="3" mol��L-1���ﵽƽ��ʱCO��ת����Ϊ60%�����ڸ��¶��£��÷�Ӧ��ƽ�ⳣ��K= ���� .
��2������ͬ�¶��£�����ʼʱc��CO��="1" mol��L-1��c��H2O��="2" mol��L-1����Ӧ����һ��ʱ����H2��Ũ��Ϊ0.5 mol��L-1�����ʱ�÷�Ӧ�Ƿ�ﵽƽ��״̬ ����ǡ��롰������ʱv������ v���棩������ڡ���С�ڡ����ڡ��������жϵ�������
��������
��3���������¶ȣ��÷�Ӧ��Kֵ�� ���÷�Ӧ�Ļ�ѧ��Ӧ���ʽ� �� �����������С�����䡱����
��1��1 ��2������ ��Ϊ��ʱ��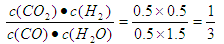 С��ƽ�ⳣ��1����������Ӧ���ʴ����淴Ӧ���ʡ�
С��ƽ�ⳣ��1����������Ӧ���ʴ����淴Ӧ���ʡ�
��3������ ��С
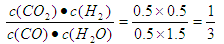 С��ƽ�ⳣ��1����������Ӧ���ʴ����淴Ӧ���ʡ�
С��ƽ�ⳣ��1����������Ӧ���ʴ����淴Ӧ���ʡ���3������ ��С
������淴Ӧ���йؼ��㼰��������Է�Ӧ���ʺ�ƽ�ⳣ����Ӱ�졣
��1�� CO��g��+H2O��g�� CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼŨ�ȣ�mol/L�� 2 3 0 0
ת����Ũ�ȣ�mol/L�� 1.2 1.2 1.2 1.2
ƽ��Ũ�ȣ�mol/L�� 0.8 1.8 1.2 1.2
����ƽ�ⳣ���ı���ʽ��֪K��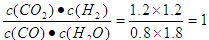
��2�� CO��g��+H2O��g�� CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼŨ�ȣ�mol/L�� 1 2 0 0
ת����Ũ�ȣ�mol/L�� 0.5 0.5 0.5 0.5
ijʱ��Ũ�ȣ�mol/L�� 0.5 1.5 0.5 0.5
��ʱ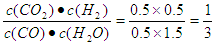 ��1
��1
����û�дﵽƽ��״̬����ʱ����Ӧ���ʴ����淴Ӧ���ʡ�
��3����Ϊ��Ӧ�Ƿ��ȷ�Ӧ�����Խ����¶ȣ�ƽ��������Ӧ�����ƶ������ƽ�ⳣ�������¶ȷ�Ӧ���ʼ�С��
��1�� CO��g��+H2O��g��
 CO2��g��+H2��g��
CO2��g��+H2��g����ʼŨ�ȣ�mol/L�� 2 3 0 0
ת����Ũ�ȣ�mol/L�� 1.2 1.2 1.2 1.2
ƽ��Ũ�ȣ�mol/L�� 0.8 1.8 1.2 1.2
����ƽ�ⳣ���ı���ʽ��֪K��
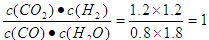
��2�� CO��g��+H2O��g��
 CO2��g��+H2��g��
CO2��g��+H2��g����ʼŨ�ȣ�mol/L�� 1 2 0 0
ת����Ũ�ȣ�mol/L�� 0.5 0.5 0.5 0.5
ijʱ��Ũ�ȣ�mol/L�� 0.5 1.5 0.5 0.5
��ʱ
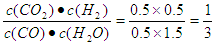 ��1
��1����û�дﵽƽ��״̬����ʱ����Ӧ���ʴ����淴Ӧ���ʡ�
��3����Ϊ��Ӧ�Ƿ��ȷ�Ӧ�����Խ����¶ȣ�ƽ��������Ӧ�����ƶ������ƽ�ⳣ�������¶ȷ�Ӧ���ʼ�С��

��ϰ��ϵ�д�
 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
�����Ŀ
 �����ô˸�������������ѧ���⣺
�����ô˸�������������ѧ���⣺ 4NO(g)��6H2O(g)�������¶ȱ��ֲ��䲢����He����ƽ�� ��������ƶ������������ƶ����������ƶ�������
4NO(g)��6H2O(g)�������¶ȱ��ֲ��䲢����He����ƽ�� ��������ƶ������������ƶ����������ƶ������� ����������� ����д���������С�����䡱����
����������� ����д���������С�����䡱���� C��g��+D��g���Ѵ�ƽ�����
C��g��+D��g���Ѵ�ƽ�����  nC��s��+D��g����ƽ�⡣��ά���¶Ȳ��䣬����ѹǿ����û�������ƽ����Է����������䣬�������ж���ȷ����( )
nC��s��+D��g����ƽ�⡣��ά���¶Ȳ��䣬����ѹǿ����û�������ƽ����Է����������䣬�������ж���ȷ����( )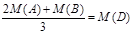
 CH3COCH2COH(CH3)2(l)��ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ����(Y-t)����ͼ��ʾ������˵����ȷ���ǣ� ��
CH3COCH2COH(CH3)2(l)��ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ����(Y-t)����ͼ��ʾ������˵����ȷ���ǣ� ��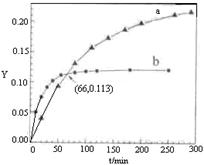
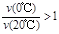
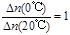
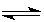 2C(g)��D(g)����һ���¶ȡ�����̶����ܱ������н��У�������������˵��������Ӧ�ﵽƽ��״̬����
2C(g)��D(g)����һ���¶ȡ�����̶����ܱ������н��У�������������˵��������Ӧ�ﵽƽ��״̬����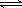 2XY2
2XY2 C(g)+2D(g)�Ѵﵽƽ��״̬�ı�־��
C(g)+2D(g)�Ѵﵽƽ��״̬�ı�־�� 2C(g) ��H="-192" kJ��mol-1����M��N�У���ͨ��x mol A��y mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䡣����˵����ȷ����
2C(g) ��H="-192" kJ��mol-1����M��N�У���ͨ��x mol A��y mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䡣����˵����ȷ����