题目内容
2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=0.2 mol·L-1·s-1 B.z=3
C.B的转化率为25% D.C的体积分数为28.6%
D
解析试题分析:A的转化率为50%,因此消耗A的物质的量是2mol×50%=1mol,而生成D的物质的量是0.25 mol·L-1·s-1×2L×2s=1mol,根据物质的量的变化量之比是相应的化学计量数之比可知,z=2,B不正确;反应速率之比是相应的化学计量数之比,因此v(C)=0.25 mol·L-1·s-1,A不正确;根据方程式可知消耗B是1.5mol,所以B的转化率是 =75%,C不正确。生成C的物质的量是1mol,所以C的体积分数=
=75%,C不正确。生成C的物质的量是1mol,所以C的体积分数= ×100%=28.6%,D正确,答案选D。
×100%=28.6%,D正确,答案选D。
考点:考查可逆反应的有关计算
点评:该题是高考中的成键题型,属于中等难度的试题,侧重对学生灵活运用基础知识解决实际问题的能力的培养,有利于培养学生的逻辑思维能力和规范答题能力。明确反应速率之比是相应的化学计量数之比是答题的关键。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g) +H2O(g)=CO(g) +3H2(g) △H>0,在一定条件下,向体积为1L的密闭容器中充入1 mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是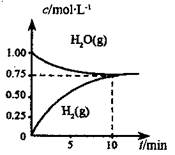
| A.达平衡时,CH4( g)的转化率为75% |
| B.0~10 min 内,v(CO)=0.075 mol?L-1·min-1 |
| C.该反应的化学平衡常数K=0.1875 mol?L-1 |
| D.当CH4(g)的消耗速率与H2O(g)的生成速率相等,反应到达平衡 |
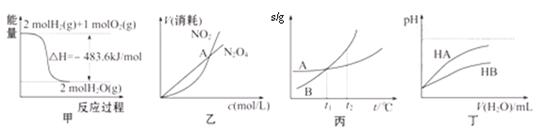
在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
| A.图甲,P1>P2,a < 3 |
| B.图甲,T1<T2,Q>0 |
| C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 |
| D.图乙,如果a=3, t2时表示向体系中加入了催化剂 |
决定化学反应速率的主要因素是 ( )
| A.反应物的浓度 | B.反应温度 |
| C.使用催化剂 | D.反应物的性质 |
一定条件下,化学反应方向的判据为:△G=△H-T△S。已知反应A(s)= D(g)+E(g),△H-T△S=(-4499+11T)J/mol,(温度单位为K)。要防止A分解反应发生,温度必须( )
| A.高于或等于409K | B.低于136K |
| C.高于136K而且低于409K | D.任意温度 |
可逆反应2NO2 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2,NO,O2表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤⑦ | C.①③④⑤ | D.全部 |
反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
| A.0.1s | B.2.5s | C.5s | D.10s |

 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动