题目内容
X2-的核外电子排布为2、8、8,则X元素在周期表中的位置是( )
| A、第三周期0族 |
| B、第三周期ⅥA族 |
| C、第三周期ⅦA族 |
| D、第四周期IA族 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:阴离子核外电子数=原子序数+离子所带电荷数,阳离子核外电子数=原子序数-离子所带电荷数,原子中核外电子数=原子序数,根据该离子的核外电子数确定原子序数,再根据该原子核外电子层数、最外层电子数确定在周期表中的位置.
解答:
解:该元素原子序数=2+8+8-2=16,所以该元素是S元素,S原子结构示意图为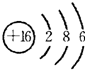 ,该原子核外有3个电子层、最外层电子数是6,所以S元素位于第三周期第VIA族,故选B.
,该原子核外有3个电子层、最外层电子数是6,所以S元素位于第三周期第VIA族,故选B.
 ,该原子核外有3个电子层、最外层电子数是6,所以S元素位于第三周期第VIA族,故选B.
,该原子核外有3个电子层、最外层电子数是6,所以S元素位于第三周期第VIA族,故选B.
点评:本题考查了原子结构,明确离子中原子序数、核外电子数、电荷数之间的关系式是解本题关键,再结合原子的电子层数、最外层电子数分析解答,题目难度不大.

练习册系列答案
相关题目
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A、反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B、氢氧化铜可溶于氨水说明氢氧化铜是两性氢氧化物 |
| C、在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3给出孤电子对 |
| D、在[Cu(NH3)4]2+离子中,Cu2+给出孤电子对,NH3提供空轨道 |
硒是人体肝脏和肾脏的组成元素之一,现在含有元素硒(Se)的保健品已经进入市场,已知它与氧元素同主族,与K同周期,关于硒的说法中不正确的是( )
| A、原子序数为34 |
| B、最高价氧化物的水化物的分子式为:H2SeO4 |
| C、Se的非金属性比Br弱 |
| D、气态氢化物的稳定性比硫化氢气体强 |
反应物A、B是无色溶液,产物AB是白色沉淀,则下列各条件下发生的反应:A+B═AB,最先看到有白色沉淀生成的是( )
| A、常温下,0.1mol?L-1的A、B溶液各10mL相混合 |
| B、在标准状况下,0.1mol?L-1的A、B溶液各l0mL相混合 |
| C、在标准状况下,100mL中含A、B各0.05mol?L-1的溶液 |
| D、常温下,20mL中含有A、B各0.003mol?L-1的溶液 |
已知在25℃、101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40kJ热量,表示上述反应的热化学方程式正确的是( )
| A、C8H18(l)+O2(g)═8CO2(g)+9H2O△H=-48.40 kJ?mol-1 |
| B、C8H18(l)+O2(g)═8CO2(g)+9H2O(l)△H=-5 518 kJ?mol-1 |
| C、C8H18(l)+O2(g)═8CO2(g)+9H2O(l)△H=+5 518 kJ?mol-1 |
| D、C8H18(l)+O2(g)═8CO2(g)+9H2O(l)△H=+48.40 kJ?mol-1 |
下列关于配位化合物的叙述中,不正确的是( )
| A、配位化合物中必定存在配位键 |
| B、配位键仅存在于配位化合物中 |
| C、[Cu(H2O)4]2+中的Cu2+提供空轨道,H2O中的氧原子提供孤对电子形成配位键 |
| D、配位化合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有着广泛的应用 |
已知t℃,KW=1×10-12,若在t℃时,某溶液中的c(H+)=1×10-7mol?L-1,则该溶液( )
| A、呈酸性 | B、呈碱性 |
| C、呈中性 | D、不确定 |
 若将有机物分子中碳、氢元素符号省略,而只表示分子中键的连接情况,每个拐点或终点均表示一个碳原子,称为键线式,如丙烷的键线式为.人体对维生素的需要量虽少,但一旦缺乏,人体就不能正常发育,还会引起疾病,下面是维生素A的结构简式:
若将有机物分子中碳、氢元素符号省略,而只表示分子中键的连接情况,每个拐点或终点均表示一个碳原子,称为键线式,如丙烷的键线式为.人体对维生素的需要量虽少,但一旦缺乏,人体就不能正常发育,还会引起疾病,下面是维生素A的结构简式: