题目内容
9. (1)在一定条件下,对于密闭容器中进行的可逆反应:2HI (g)?H2(g)+I2(g),下列说法中,能说明这一反应已经达到化学反应限度的是D
(1)在一定条件下,对于密闭容器中进行的可逆反应:2HI (g)?H2(g)+I2(g),下列说法中,能说明这一反应已经达到化学反应限度的是DA.正、逆反应速率都等于零
B.HI、H2、I2的浓度相等
C.HI、H2、I2在容器中共存
D.HI、H2、I2的浓度均不再变化
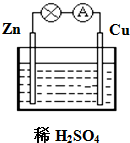
(2)对于铜-锌原电池,以下说法不正确的是D
A.铜为正极
B.锌片上发生氧化反应
C.它是一种把化学能转化为电能的装置
D.铜片向外电路提供电子,锌片从外电路得到电子
该电池的正极的电极反应式是2H++2e-=H2↑.
(3)氯化铵溶液的PH小于7(填“大于”,“小于”,“等于”),原因是NH4++H2O?NH3.H2O+H+(用离子方程式表示)
(4)已知25℃,101KPa时,1g氢气完全燃烧放出aKJ的热量,下列氢气燃烧的热化学方程式正确的是B
A.2H2(g)+O2(g)═2H2O(l)△H=-2a KJ∕mol
B.2H2(g)+O2(g)═2H2O(l)△H=-4a KJ∕mol
C.2H2(g)+O2(g)═2H2O(l)△H=+2a KJ∕mol
D.2H2(g)+O2(g)═2H2O(l)△H=+4a KJ∕mol.
分析 (1)可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的物理量不变,据此分析解答;
(2)锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应;电子从负极沿导线流向正极,据此分析;
(3)NH4Cl是强酸弱碱盐,铵根离子水解导致溶液的pH值<7;
(4)1g氢气完全燃烧放出aKJ的热量,所以2mol氢气也就是4g氢气完全燃烧放出4aKJ的热量.
解答 解:(1)A.化学平衡状态,正逆反应速率相等,但不为0,反应也没有停止,是一个动态平衡,故A错误;
B.HI、H2、I2的浓度相等时该反应不一定达到平衡状态,与反应物的量及转化率有关,故B错误;
C.只要是可逆反应,无论该反应是否达到平衡状态,HI、H2、I2都在密闭容器中共存,所以不能据此判断平衡状态,故C错误;
D.HI、H2、I2的浓度不再发生变化时,正逆反应速率相等,该反应达到平衡状态,故D正确;
故选D;
(2)A、锌、铜和稀硫酸组成的原电池中,活泼性弱的金属铜作正极,故A正确;
B、锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应,故B正确;
C、该装置为原电池,是一种把化学能转化为电能的装置,故C正确;
D、锌作负极失电子,所以电子从Zn流向Cu,故D错误;
正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,
故答案为:D;2H++2e-=H2↑;
(3)NH4Cl是强酸弱碱盐,铵根离子水解导致溶液的pH值<7,水解方程式为NH4++H2O?NH3.H2O+H+,故答案为:小于;NH4++H2O?NH3.H2O+H+;
(4)1g氢气完全燃烧放出aKJ的热量,所以2mol氢气也就是4g氢气完全燃烧放出4aKJ的热量,所以热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-4a KJ∕mol,故选B.
点评 本题考查化学平衡状态的判断、原电池原理和热化学方程式的书写原则,(2)题要明确正负极上得失电子是解本题关键,难度不大,难点是电极反应式的书写.

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案| A. | X-a | B. | X-a-n | C. | X-a+n | D. | X+a-n |
| A. | 根据酸分子中含有H原子个数将酸分为一元酸、二元酸 | |
| B. | 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素 | |
| D. | 根据分散系的稳定性大小将混合物分为胶体、溶液和浊液 |
| A. | 得到电子 | B. | 失去电子 | C. | 得到质子 | D. | 失去中子 |
| A. | 用纯锌与稀硫酸反应 | |
| B. | 用粗锌与稀硫酸反应 | |
| C. | 用粗锌与稀硝酸反应 | |
| D. | 在CuSO4溶液中浸泡过的纯锌与稀硫酸反应 |
 .
.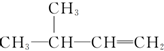 3-甲基-1-丁烯
3-甲基-1-丁烯 3-甲基-2-丁醇.
3-甲基-2-丁醇.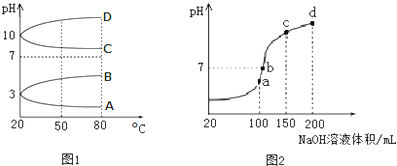
 ,该反应类型是加聚反应.
,该反应类型是加聚反应.