题目内容
【题目】各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。

请回答下列问题:
(1)G元素在周期表中的位置______________________,C的电子式______________。
(2)比较Y与Z的原子半径大小:___________________(填写元素符号)。
(3)写出E和乙醛反应的化学反应方程式(有机物用结构简式表示):___________________________;
反应类型:_____。
(4)写出实验室制备G的离子反应方程式:_______________________。
(5)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为____________。
(6)实验室中检验L溶液中的阳离子常选用__________(填化学式)溶液,现象是______________。
(7)A中包含X、Y、Z元素,A的化学式为_____________。
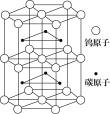
(8)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其一种同素异形体的名称_______________________________________、__________________。
【答案】 第3周期ⅦA族 ![]() C O CH3CHO+2Cu(OH)2+NaOH
C O CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O 氧化反应 MnO2 + 4H+ + 2Cl-
CH3COONa+Cu2O↓+3H2O 氧化反应 MnO2 + 4H+ + 2Cl-![]() Mn2+ + Cl2↑+ 2H2O 纯碱(或苏打) KSCN 溶液变血红色 Cu2(OH)2CO3 金刚石 石墨(足球烯)
Mn2+ + Cl2↑+ 2H2O 纯碱(或苏打) KSCN 溶液变血红色 Cu2(OH)2CO3 金刚石 石墨(足球烯)
【解析】(1)X在周期表中的原子半径最小,为H;C(H2O)、D由X(H)、Y、Z中两种元素组成,则Y、Z中有氧(O),再结合Y、Z原子最外层电子数之和为10,X、Y、Z的原子序数依次增大,可以确定Z为氧(O)、Y为碳(C)。进而推出D(由H、C、O中的两种元素组成;无色非可燃性气体)为CO2。最后,从A+H(HCl)=B(CuCl2)+C(H2O)+D(CO2)可知,A是含有Cu2+的碳酸盐,所以A是CuCO3或Cu2(OH)2CO3; G为黄绿色单质气体,G为氯元素,所在周期表中的位置为第3周期ⅦA族; C为H2O,水的电子式为:![]() ;(2)Y与Z分别是C、O,依据同周期原子半径依次减小判断,C、O的原子半径C>O;(3)依据判断可知,反应②是葡萄糖和氢氧化铜加热反应,反应的化学方程式为:CH3CHO+2Cu(OH)2+NaOH
;(2)Y与Z分别是C、O,依据同周期原子半径依次减小判断,C、O的原子半径C>O;(3)依据判断可知,反应②是葡萄糖和氢氧化铜加热反应,反应的化学方程式为:CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O;属于氧化反应;(4)实验室用浓盐酸与二氧化锰在加热条件下反应制备氯气的离子反应方程式为:MnO2 + 4H+ + 2Cl-
CH3COONa+Cu2O↓+3H2O;属于氧化反应;(4)实验室用浓盐酸与二氧化锰在加热条件下反应制备氯气的离子反应方程式为:MnO2 + 4H+ + 2Cl-![]() Mn2+ + Cl2↑+ 2H2O ;(5)二氧化碳气体与NaOH溶液反应可生成两种盐碳酸钠和碳酸氢钠,其中碳酸钠中Na的质量分数为43%,其俗名为纯碱或苏打;(6)实验室中检验氯化铁溶液中的阳离子铁离子常选用KSCN溶液,现象是溶液变血红色;(7)A中包含X、Y、Z元素,A的化学式为Cu2(OH)2CO3;(5)CO2可以还原成正四面体结构的晶体N,即化合价降低,显然生成了金刚石,它的同素异形体必须为含碳的单质,同素异形体的名称为:金刚石、如石墨、富勒烯(C60)等。
Mn2+ + Cl2↑+ 2H2O ;(5)二氧化碳气体与NaOH溶液反应可生成两种盐碳酸钠和碳酸氢钠,其中碳酸钠中Na的质量分数为43%,其俗名为纯碱或苏打;(6)实验室中检验氯化铁溶液中的阳离子铁离子常选用KSCN溶液,现象是溶液变血红色;(7)A中包含X、Y、Z元素,A的化学式为Cu2(OH)2CO3;(5)CO2可以还原成正四面体结构的晶体N,即化合价降低,显然生成了金刚石,它的同素异形体必须为含碳的单质,同素异形体的名称为:金刚石、如石墨、富勒烯(C60)等。