题目内容
硝酸工业中尾气的N的氧化物(NO,NO2)是主要的大气污染之一,其常用的治理方法中有以下两种(已简化)。
① NaOH吸收法,反应原理如下:
2NO2+2NaOH=NaNO3+NaNO2+H2O
② 氨催化还原法,反应原理是:

现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体),若用过量的NaOH吸收后,溶液中NaNO3和NaNO2的物质的量之比恰好与原尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
x=__________________________________________。
(2)将1体积的该尾气用②的方法处理,至少消耗相同状况下的NH3的体积为____________。
(3)配平下列方程式:
______NOx+_____NH3=______N2+_____H2O
① NaOH吸收法,反应原理如下:
2NO2+2NaOH=NaNO3+NaNO2+H2O
② 氨催化还原法,反应原理是:

现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体),若用过量的NaOH吸收后,溶液中NaNO3和NaNO2的物质的量之比恰好与原尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
x=__________________________________________。
(2)将1体积的该尾气用②的方法处理,至少消耗相同状况下的NH3的体积为____________。
(3)配平下列方程式:
______NOx+_____NH3=______N2+_____H2O
(1)1.75 (2)1.17 (3)3,2x,(3+2x)/2,3x
(1)由反应方程式及题意,设n(NO2)∶n(NO)=k(k>1)
又设:NO为1mol,则NO2为kmol。
NO+NO2+2NaOH=2NaNO2+H2O
1 1 2
应有NO消耗量为1mol,生成NaNO2为2mol,余NO2为(k-1)mol。
2NO2+2NaOH====NaNO2+NaNO3+H2O
2 1 1
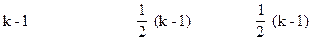

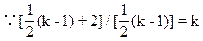
∴k=3即n(NO2)∶n(NO)=3∶1
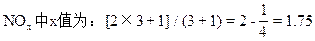
(2)由方程式:
NOx+yNH3→N2↑+xH2O
由含氧量守恒有:2x=3y
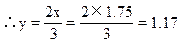
(3)用1,n法配平:首先NOx前系数定为1,NH3前为n。
利用原子个数守恒,配平N、H元素:
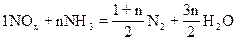
∵“O”原子个数守恒:
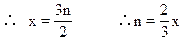
把n值代回原式,有:
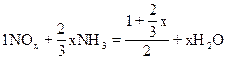
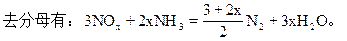
又设:NO为1mol,则NO2为kmol。
NO+NO2+2NaOH=2NaNO2+H2O
1 1 2
应有NO消耗量为1mol,生成NaNO2为2mol,余NO2为(k-1)mol。
2NO2+2NaOH====NaNO2+NaNO3+H2O
2 1 1
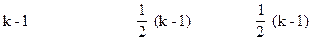

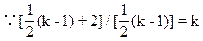
∴k=3即n(NO2)∶n(NO)=3∶1
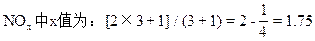
(2)由方程式:
NOx+yNH3→N2↑+xH2O
由含氧量守恒有:2x=3y
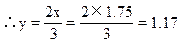
(3)用1,n法配平:首先NOx前系数定为1,NH3前为n。
利用原子个数守恒,配平N、H元素:
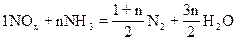
∵“O”原子个数守恒:
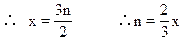
把n值代回原式,有:
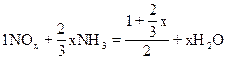
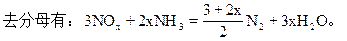

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目