题目内容
X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如下表,W与R是同族元素。
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
回答下列有关问题:
W原子的价电子排布图为_______________________________。
化合物Q2W2的电子式_________________,化合物XYZ的结构式________________。
Y、Z、W分别与X形成常见化合物的沸点由高到低的顺序是____________________(用分子式表示)。
RW3分子中的键角___________,W3分子的立体构型是_______________形。
根据等电子原理,指出与YW2互为等电子体且含有Z原子的微粒有 、
(要求写一种分子和一种离子)。
(1) ![]() (2分)
(2分)
(2) ![]() (2分) H-C≡N(2分)
(2分) H-C≡N(2分)
(3) H2O>NH3>CH4 (2分)
(4) 120˚ V(各1分)
(5) N2O(1分)N3-(或OCN-、SCN-、NO2+)(1分)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
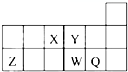 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )| A、元素Y最高正化合价与最低负化合价的绝对值之和的数值等于8 | B、原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q) | C、离子Y2-和Z3+半径的大小顺序为:r(Y2-)>r(Z3+) | D、元素W的最高价氧化物对应的水化物的酸性比Q的强 |
 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的( ) (2012?天津模拟)短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )
(2012?天津模拟)短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )