题目内容
【题目】高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是

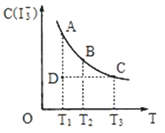
A. 该反应过程中的能量变化如图所示
B. 该反应条件下,Al的还原性弱于Fe
C. 1molFe3O4参与反应转移8×6.02×1023个电子
D. 实验室进行该反应时常加入KClO3作催化剂
【答案】C
【解析】A.铝热反应属于放热反应,反应物的总能量大于生成物的总能量,图象不符,A错误;B.Al和Fe3O4反应生成Fe和Al2O3,Al作还原剂,Fe是还原产物,所以Al的还原性强于Fe,B错误;C.反应中Fe元素的化合价从+8/3价降低到0价,所以反应中每消耗1 mol Fe3O4转移8×6.02×1023个电子,C正确;D.铝热反应中氯酸钾受热分解生成氧气,反应中KClO3不是催化剂,D错误,答案选C。

练习册系列答案
相关题目