题目内容
根据元素周期律和物质结构的有关知识,以下有关排序正确的是( )
A. 离子半径:Ca2+>Cl->S2-
B. 第一电离能:Si>C>N
C. 电负性:F>S>Mg
D. 热稳定性:SiH4>H2S>H2O
某化学兴趣小组用下面所示装置制取氯酸钾、次氯酸钠和氯水并进行探究实验。

实验I.制取氮酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学反应方程式________________________________。
(2)制取实验结束后,取出装置B中的试管,冷却结晶、过滤、洗涤,该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、_________、_________。为提高氯酸钾和次氯酸钠的产率,在实验装置中还需要改进的是_________。
(3)装置 C 中反应需要在冰水浴中进行,其原因是________________________________。
(4)装置D中的实验现象是溶液先变红后褪色,最后又变为_________色。
实验Ⅱ 尾气处理
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(5)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中的CO2的影响)
①提出合理假设
假设1:只存在SO32- ;假设2:既不存在SO32-也不存在ClO-;假设 3:_________。
②设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3mol/L H2SO4、1mol/LNaOH 溶液、0.01mol/L 酸性 KMnO4 溶液、淀粉 KI 溶液。
实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液分置于A、B试管中 | |
步骤2:向A试管中滴加0.01mol/L酸性 | (1)若溶液褪色,则假设1成立 |
KMnO4溶液 | (2)若溶液不褪色,则假设2或3成立 |
步骤3:_____ | _____ |






 2NH3的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强
2NH3的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强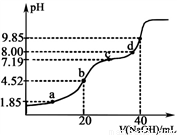
 溶液中:2c(H2SO3)+c(SO32-)=0.1 mol·L?1
溶液中:2c(H2SO3)+c(SO32-)=0.1 mol·L?1
 NH3↑+HCl↑
NH3↑+HCl↑