题目内容
对于在一固定容积容器中发生的反应:2SO2(g)+O2(g)?2SO3(g)(正反应为放热反应)下列措施中,既可加快反应速率,又可使平衡右移的是( )
分析:根据外界条件对化学反应速率的影响分析,增大浓度、升高温度、增大压强、使用催化剂等可以加快反应速率,结合平衡移动原理分析解答.
解答:解:A.通入氧气,氧气浓度增大,反应速率加快,平衡向正反应方向移动,故A符合;
B.减小压强平衡向逆反应方向移动,反应速率减慢,故B不符合;
C.使用催化剂,加快反应速率,但不影响平衡移动,故C不符合;
D.降低温度平衡向正反应方向移动,但反应速率减慢,故D不符合;
故选A.
B.减小压强平衡向逆反应方向移动,反应速率减慢,故B不符合;
C.使用催化剂,加快反应速率,但不影响平衡移动,故C不符合;
D.降低温度平衡向正反应方向移动,但反应速率减慢,故D不符合;
故选A.
点评:本题考查外界条件对化学反应速率与化学平衡的影响,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
对于在一固定容积容器中发生的反应:2SO2(g)+ O2(g)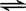 2SO3(g)(正反应为放热反应),下列措施中,既可加快反应速率,又可使平衡向右移动的是
2SO3(g)(正反应为放热反应),下列措施中,既可加快反应速率,又可使平衡向右移动的是
| A.降温 | B.减压 | C.加催化剂 | D.增加O2 |
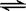 2SO3(g)(正反应为放热反应),下列措施中,既可加快反应速率,又可使平衡向右移动的是
2SO3(g)(正反应为放热反应),下列措施中,既可加快反应速率,又可使平衡向右移动的是