题目内容
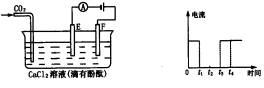
下图为持续电解含一定CaCl2水溶液的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入电解液中。
(1)电解时,F极发生_______________反应,电极反应式为_______________,E极发生_______________反应,电极反应式为______________________________,电解总反应的离子方程式为______________________________。
(2)电解池中产生的现象:
①_________________________________________________________________;
②_________________________________________________________________;
③_________________________________________________________________。
解析:F极与电源正极相连接,是电解池中的阳极,Cl-在此发生氧化反应生成Cl2;E极是电解池的阴极,H+在此发生还原反应生成H2,随着H+的不断反应,水的电离平衡正向移动使E极附近H+浓度小于OH-浓度,溶液呈碱性,使酚酞变红色;电解的总化学方程式为CaCl2+2H2O![]() Ca(OH)2+Cl2↑+H2↑;电解一段时间后,通CO2发生的反应有CO2+Ca(OH)2
Ca(OH)2+Cl2↑+H2↑;电解一段时间后,通CO2发生的反应有CO2+Ca(OH)2 ![]() CaCO3↓+H2O、CaCO3+CO2+H2O
CaCO3↓+H2O、CaCO3+CO2+H2O![]() Ca(HCO3)2。
Ca(HCO3)2。
答案:(1)氧化 2Cl--2e-![]() Cl2↑ 还原 2H++2e-
Cl2↑ 还原 2H++2e-![]() H2↑ 2Cl-+2H2O
H2↑ 2Cl-+2H2O![]() 2OH-+H2↑ +Cl2↑
2OH-+H2↑ +Cl2↑
(2)①通电后E极处溶液呈红色
②通电时,E极、F极均有气体生成
③通CO2时,溶液中先出现白色沉淀,继续通CO2沉淀又消失

下图为持续电解含一定CaCl2水溶液的装置(以铂为电极),A为电流表,电解一段时间t1后,将CO2连续通入电解液中,请在右下图中完成左下图实验中电流对时间的变化关系图,并填空回答:
 |

(1)电解时,F极发生 反应,电极反应式为 ;E极发生 反应,电极反应式为 ,电解总反应式 。
(2)电解池中产生的现象:① ;② ;③ 。