题目内容
药品:稀硫酸、浓硫酸、氧化铜,
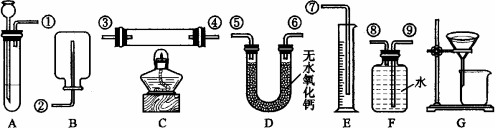
实验装置:另有托盘天平可用,
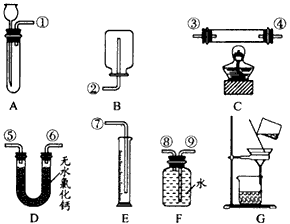
(1)你选用的药品是____。
(2)你选用的实验装置有___(填装置编号)。若需要组装,则连接的顺序是____(用装置接口处的编号表示。若不需要组装,则不填)。
(3)称取ag黄铜粉样品进行实验,实验中测定的 其他有效数据是___。
A.标准状况下,生成H2的体积bL
B.反应前仪器和药品的质量cg
C.反应后剩余固体的质量dg
D.反应后仪器和药品的质量eg
(4)计算合金中锌的质量分数____ 。
(2)方案一:A、E、F; 方案二:A; 方案三:A、G ①⑧⑨⑦
(3)方案一:A; 方案二:B、D; 方案三:C
(4)方案一:
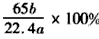 ; 方案二:
; 方案二: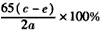 ; 方案三:
; 方案三: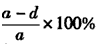

 阅读快车系列答案
阅读快车系列答案
| |||||||||||||||||||
某学生要用50 mL NaOH溶液和CO2来制取纯Na2CO3溶液,已知CO2气体在通入NaOH溶液过程中极易生成NaHCO3,且无明显现象。
实验室有下列试剂:①未知浓度的NaOH溶液 ②37%的盐酸 ③37%的硫酸 ④14%的盐酸 ⑤大理石⑥饱和NaHCO3溶液
实验室有下列仪器:量筒,烧杯,橡皮管,玻璃导管,分液漏斗,烧杯,洗气瓶,酒精灯。
已知下表中各物质在常温时的溶解度(g/100 g H2O)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
本实验除了下面图给的仪器外,还应有: (仪器安装补完整)。
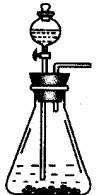
实验为保证制得Na2CO3的纯度,应选用的药品,除①外,还应需要: 。
简要叙述实验步骤,直到制得纯碳酸钠溶液 。
根据给出的溶解度表,若保证在配制过程中不会有晶体析出,所用氢氧化钠溶液中含NaOH的质量分数的最大值是多少(写出计算步骤和必要的文字说明)?
某学生要用50 mL NaOH溶液和CO2来制取纯Na2CO3溶液,已知CO2气体在通入NaOH溶液过程中极易生成NaHCO3,且无明显现象。
实验室有下列试剂:①未知浓度的NaOH溶液 ②37%的盐酸 ③37%的硫酸 ④14%的盐酸 ⑤大理石⑥饱和NaHCO3溶液
实验室有下列仪器:量筒,烧杯,橡皮管,玻璃导管,分液漏斗,烧杯,洗气瓶,酒精灯。
已知下表中各物质在常温时的溶解度(g/100 g H2O)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
本实验除了下面图给的仪器外,还应有: (仪器安装补完整)。
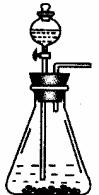
实验为保证制得Na2CO3的纯度,应选用的药品,除①外,还应需要: 。
简要叙述实验步骤,直到制得纯碳酸钠溶液 。
根据给出的溶解度表,若保证在配制过程中不会有晶体析出,所用氢氧化钠溶液中含NaOH的质量分数的最大值是多少(写出计算步骤和必要的文字说明)?