题目内容
【题目】25℃时,用浓度为0.1000mol/L的氢氧化钠溶液分别滴定20. 00mL浓度均为0.l000mol/L的两种酸HX、HY(忽略体积变化),实验数据如下表,下列判断不正确的是
数据编号 | 滴入NaOH(aq) 的体积/mL | 溶液的pH | |
HX | HY | ||
① | 0 | 3 | 1 |
② | a | 7 | x |
③ | 20.00 | >7 | y |
A. 在相同温度下,同浓度的两种酸溶液的导电能力:HX<HY
B. 由表中数据可估算出Ka(HX)≈10-5
C. HY和HX混合,c(H+)=c(X一)+c(Y一)+c(OH一)
D. 上述②反应后的HY溶液中:c(Na+)>c(Y一)>c(OH一)>c(H+)
【答案】D
【解析】试题分析:A.0.1000molL-1的酸HX、HY的pH分别为3、1,可知HX为弱酸、HY为强酸,HY溶液中离子浓度更大,同浓度的两种酸溶液的导电能力顺序HX<HY,A正确;B.0.100mol/L的HX溶液的pH=3,则c(H+)≈c(X-)=10-3mol/L,c(HX)=0.1mol/L-c(X-)≈0.1mol/L,则Ka(HX)=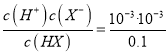 =10-5,B正确;C.HY和HX混合,根据电荷守恒:c(H+)=c(X-)+c(Y-)+c(OH-),C正确;D.上述②反应后的HX溶液显中性,因为HX为弱酸,则a<20.00 mL,由于HY为强酸,故HY酸过量,c(H+)>c(OH-),结合电荷守恒可知:c(Y-)>c(Na+),溶液中正确的离子浓度大小为:c(Y-)>c(Na+)>c(H+)>c(OH-),D错误;答案选D。
=10-5,B正确;C.HY和HX混合,根据电荷守恒:c(H+)=c(X-)+c(Y-)+c(OH-),C正确;D.上述②反应后的HX溶液显中性,因为HX为弱酸,则a<20.00 mL,由于HY为强酸,故HY酸过量,c(H+)>c(OH-),结合电荷守恒可知:c(Y-)>c(Na+),溶液中正确的离子浓度大小为:c(Y-)>c(Na+)>c(H+)>c(OH-),D错误;答案选D。

【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. A B. B C. C D. D