题目内容
 (2010?泰州三模)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
(2010?泰州三模)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:步骤Ⅰ:称取0.4g花生油样品,置于两个干燥的碘瓶(如图)内,加入10mL四氯化碳,轻轻摇动使油全部溶解.向碘瓶中加入25.00mL含0.01mol IBr的无水乙酸溶液,盖好瓶塞,在玻璃塞与瓶口之间滴加数滴10%碘化钾溶液封闭缝隙,以免IBr的挥发损失.
步骤Ⅱ:在暗处放置30min,并不时轻轻摇动.30min后,小心地打开玻璃塞,用新配制的10%碘化钾10mL和蒸馏水50mL把玻璃塞和瓶颈上的液体冲洗入瓶内.
步骤Ⅲ:加入指示剂,用0.1mol?L-1硫代硫酸钠溶液滴定,用力振荡碘瓶,直至终点.
测定过程中发生的相关反应如下:
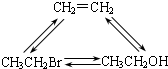
①

②IBr+KI=I2+KBr
③I2+2S2O32-=2I-+S4O62-
请回答下列问题:
(1)已知卤素互化物IBr的性质与卤素单质类似,实验中准确量取IBr溶液应用
酸式滴定管
酸式滴定管
,用方程式表示碘瓶必须干燥的原因IBr+H2O=HIO+HBr
IBr+H2O=HIO+HBr
.(2)步骤Ⅱ中碘瓶在暗处放置30min,并不时轻轻摇动的原因是
碘瓶置于暗处可减少溴化氢挥发,不断搅动可以让物质间充分反应
碘瓶置于暗处可减少溴化氢挥发,不断搅动可以让物质间充分反应
.(3)步骤Ⅲ中所加指示剂为
淀粉溶液
淀粉溶液
,滴定终点的现象溶液由蓝色恰好变为无色且30秒内不变化
溶液由蓝色恰好变为无色且30秒内不变化
.(4)反应结束后从液体混合物中回收四氯化碳,则所需操作有
分液、蒸馏
分液、蒸馏
.分析:(1)卤素互化物IBr的性质与卤素单质类似,具有氧化性,腐蚀橡胶管;IBr易发生水解反应;
(2)根据溴化氢易挥发以及使物质充分混合反应的做法来分析;
(3)根据淀粉的特性来选择试剂;
(4)反应结束后从液体混合物中回收四氯化碳的方法是先分液得到四氯化碳,再利用蒸馏的方法得到纯净的四氯化碳.
(2)根据溴化氢易挥发以及使物质充分混合反应的做法来分析;
(3)根据淀粉的特性来选择试剂;
(4)反应结束后从液体混合物中回收四氯化碳的方法是先分液得到四氯化碳,再利用蒸馏的方法得到纯净的四氯化碳.
解答:解:(1)卤素互化物IBr的性质与卤素单质类似,具有氧化性,腐蚀橡胶管,不能用碱式滴定管盛装,IBr易发生水解反应,反应方程式为:IBr+H2O=HIO+HBr,故答案为:酸式滴定管(或移液管 );IBr+H2O=HIO+HBr;
(2)溴化氢易挥发,置于暗处可减少溴化氢挥发,为使反应充分进行,应不断搅动使物质充分接触而反应,
故答案为:碘瓶置于暗处可减少溴化氢挥发,不断搅动可以让物质间充分反应;
(3)碘遇淀粉变蓝色,可用淀粉为反应的指示剂,滴定时终点的判断为 溶液由蓝色恰好变为无色且30秒内不变化,
故答案为:淀粉溶液;溶液由蓝色恰好变为无色且30秒内不变化;
(4)反应结束后从液体混合物中回收四氯化碳的方法是先分液得到四氯化碳,再利用蒸馏的方法得到纯净的四氯化碳,
故答案为:分液、蒸馏.
(2)溴化氢易挥发,置于暗处可减少溴化氢挥发,为使反应充分进行,应不断搅动使物质充分接触而反应,
故答案为:碘瓶置于暗处可减少溴化氢挥发,不断搅动可以让物质间充分反应;
(3)碘遇淀粉变蓝色,可用淀粉为反应的指示剂,滴定时终点的判断为 溶液由蓝色恰好变为无色且30秒内不变化,
故答案为:淀粉溶液;溶液由蓝色恰好变为无色且30秒内不变化;
(4)反应结束后从液体混合物中回收四氯化碳的方法是先分液得到四氯化碳,再利用蒸馏的方法得到纯净的四氯化碳,
故答案为:分液、蒸馏.
点评:本题考查氯素互化物性质的知识和实验化学两部分知识,题目较为综合,具有一定难度,做题时注意实验操作和物质性质的分析判断.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
 (2010?泰州三模)下列描述错误的是( )
(2010?泰州三模)下列描述错误的是( )