题目内容
17.已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:A$→_{一定条件}^{+D}$B$→_{一定条件}^{+D}$C(1)D是具有氧化性的气体单质
①若A是一种活泼金属单质,则化合物C的用途之一为呼吸面具或潜水艇中的供氧剂.
②若A是一种固态非金属单质,化合物B、C的相对分子质量之比为7:11,则实验室制取C的反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O.
③若A是能使湿润的红色石蕊试纸变蓝的气体,则A转化为B反应的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(2)若D是一种常见金属单质
①若A 是一种黄绿色气体,贮存溶液C时应加入少量D,其理由是(用离子方程式说明)2Fe3++Fe═3Fe2+.
②若A是一种强氧化性酸,则B的化学式为Fe(NO3)3或Fe2(SO4)3.
(3)若D是一种常见的温室气体,A是一种强碱.则B转化为C的离子方程式为CO2+CO32-+H2O=2HCO3-.
分析 (1)D是具有氧化性的气体单质可以为常见的氧气、氯气等,
①若A是一种活泼金属单质,则符合转化关系的为钠和氧气反应生成氧化钠,氧化钠和氧气反应生成过氧化钠;
②若A是一种固态非金属单质,实现上述转化,非金属元素具有变价,生成的氧化物为一氧化碳和二氧化碳,满足化合物B、C的相对分子质量之比为7:11;
③若A是能使湿润的红色石蕊试纸变蓝的气体,判断为NH3,则氨气和氧气催化剂加热反应生成一氧化氮和水;
(2)若D是一种常见金属单质
①若A 是一种黄绿色气体为Cl2,实现上述转化说明金属具有变价,符合关系的为铁,氯气和铁反应生成氯化铁,铁在水溶液中和氯化铁反应生成氯化亚铁,贮存溶液C时应加入少量D是为了防止氯化亚铁被氧化;
②若A是一种强氧化性酸,D为金属是变价金属,判断为铁,铁和硝酸,浓硫酸加热都可以反应实现上述转化关系;
(3)若D是一种常见的温室气体判断为二氧化碳,A是一种强碱,则二氧化碳和强碱反应生成正盐,二氧化碳和正盐反应会生成酸式盐,可以实现上述转化.
解答 解:(1)D是具有氧化性的气体单质可以为常见的氧气、氯气等,
①若A是一种活泼金属单质,则符合转化关系的为钠和氧气反应生成氧化钠,氧化钠和氧气反应生成过氧化钠,Na$\stackrel{O_{2}}{→}$Na2O$\stackrel{O_{2}}{→}$Na2O2,过氧化钠的用途可以做呼吸面具或潜水艇中的供氧剂,也可以做漂白剂,
故答案为:呼吸面具或潜水艇中的供氧剂;
②若A是一种固态非金属单质,实现上述转化,非金属元素具有变价,生成的氧化物为一氧化碳和二氧化碳,C$\stackrel{O_{2}}{→}$CO$\stackrel{O_{2}}{→}$CO2,满足化合物B、C的相对分子质量之比为7:11,实验室制取CO2的反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
③若A是能使湿润的红色石蕊试纸变蓝的气体,判断为NH3,则氨气和氧气催化剂加热反应生成一氧化氮和水,反应的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)若D是一种常见金属单质
①若A 是一种黄绿色气体为Cl2,实现上述转化说明金属具有变价,符合关系的为铁,氯气和铁反应生成氯化铁,铁在水溶液中和氯化铁反应生成氯化亚铁,贮存溶液C时应加入少量D是为了防止氯化亚铁被氧化,发生反应的离子方程式:Fe+2Fe3+=3Fe2+,
故答案为:Fe+2Fe3+=3Fe2+;
②若A是一种强氧化性酸,D为金属是变价金属,判断为铁,铁和硝酸反应生成硝酸铁、一氧化氮和水,硝酸铁和铁反应生成硝酸亚铁,铁和浓硫酸加热生成硫酸铁、二氧化硫和水,硫酸铁和铁反应生成硫酸亚铁,都可以反应实现上述转化关系,B的化学式为:Fe(NO3)3 或Fe2(SO4)3,
故答案为:Fe(NO3)3 或Fe2(SO4)3;
(3)若D是一种常见的温室气体判断为二氧化碳,A是一种强碱,则二氧化碳和强碱反应生成正盐,二氧化碳和正盐反应会生成酸式盐,NaOH$\stackrel{CO_{2}}{→}$Na2CO3$\stackrel{CO_{2}}{→}$NaHCO3,可以实现上述转化,B转化为C的离子方程式为:CO2+CO32-+H2O=2HCO3-,
故答案为:CO2+CO32-+H2O=2HCO3-.
点评 本题考查了无机物性质的分析判断,主要是转化关系的理解应用,掌握基础是解题关键,题目难度中等.

| A. | K+、Ag+、NO3-、Cl- | B. | NH4+、Ba2+、Cl-、CO32- | ||
| C. | Na+、Ca2+、HCO3-、NO3- | D. | K+ Fe3+ Cl- SO42 |
| A. | 原子半径A>B>D>C | B. | 原子序数d>c>b>a | ||
| C. | 离子半径C3->D->B+>A2+ | D. | a=c-5 |
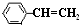 )的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯;⑤能发生硝化反应;⑥所有的原子可能共平面.其中正确的是( )
)的下列叙述中:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯;⑤能发生硝化反应;⑥所有的原子可能共平面.其中正确的是( )| A. | ①②③④⑤ | B. | ①②⑤⑥ | C. | ①②④⑤⑥ | D. | 全部正确 |
| A. | Na2O2 | B. | Ca( ClO)2 | C. | FeSO4 | D. | 浓盐酸 |
| A. | CO2的电子式: | |
| B. | 1mol Na2O2中阴、阳离子总数为4NA | |
| C. | NaOH是离子化合物,含有离子键和共价键 | |
| D. | 28g C2H4中含有4NA对共用电子对 |
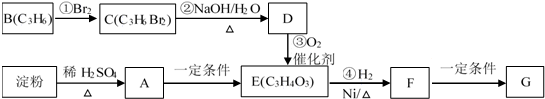
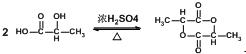 .
.