题目内容
【题目】下列说法正确的是
A. 呈酸性的雨水就是酸雨 B. 能电离出H+的物质属于酸
C. “雷雨肥庄稼”符合科学道理 D. 白色物质引起的污染叫白色污染
【答案】C
【解析】
A. pH小于5.6的雨水是酸雨,因此呈酸性的雨水不一定就是酸雨,A错误;
B. 能电离出H+的物质不一定属于酸,例如NaHSO4等,B错误;
C. “雷雨肥庄稼”过程中氮气转化为NO,NO转化为NO2,NO2与水反应转化为硝酸,硝酸与土壤中的矿物质结合转化为硝酸盐而被吸收,因此符合科学道理,C正确;
D. 白色污染是人们对难降解的塑料垃圾(多指塑料袋)污染环境现象的一种形象称谓,因此不一定是白色物质引起的污染,D错误;
答案选C。

【题目】下列物质分类的正确组合是
分类组合 | 纯净物 | 碱 | 盐 | 碱性氧化物 |
A | 碱石灰 | 氢氧化钡 | 苏打 | 氧化铝 |
B | H2O2 | 纯碱 | 小苏打 | 氧化镁 |
C | 水煤气 | NH3·H2O | 苛性钠 | 氧化钙 |
D | 五水硫酸铜 | 氢氧化钠 | 碱式碳酸铜 | 氧化钠 |
A. A B. B C. C D. D
【题目】软锰矿的主要成分为MnO2,含少量Al2O3和SiO2。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下(中间产物的固体部分已经略去)。
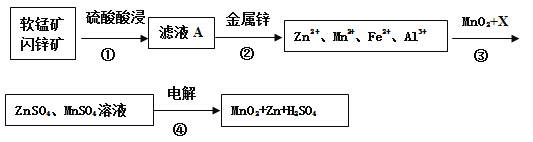
已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是_________________(任写一种)。①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式______________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_________。
(3)步骤③中MnO2的其作用是__________________,另外一种物质X可以是__________。
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式__________。
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为__________________。在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______。[已知:Ksp(MnS)=1.4×10―15]